Дефект межжелудочковой перегородки
Содержание:
Как диагностируется гипертрофическая кардиомиопатия?
Электрокардиограмма (ЭКГ). Визуальные тесты, которые могут помочь врачу определить данное состояние, включают МРТ, рентгенографию грудной клетки и эхокардиограмму.
УЗИ сердца. Сердце будет оцениваться на наличие признаков обструкции клапана, на толщину сердечной мышцы, размер камеры, диапазон движения клапана и кровоток.
Анализ крови. Образцы крови могут помочь идентифицировать определенные генные мутации.
Наблюдение за тем, как организм реагирует на физические нагрузки, является способом проверки состояния сердца. Наблюдение проводится во время или сразу после тренировки или в обоих случаях.
Стресс-тест на беговой дорожке контролирует сердечный ритм, артериальное давление и дыхание во время ходьбы или бега человека.
Тест на потребление кислорода измеряет использование кислорода пациентом, когда он использует маску во время тренировки.
Катетеризация сердца включает в себя вставку мягкой тонкой трубки, называемой катетером, в бедренную артерию. Катетер будет направлен в восходящую аорту и левый желудочек сердца, чтобы измерить разницу давления между ними. У человека с гипертрофической кардиомиопатией давление будет отличаться.
Кардиомиопатия: симптомы
Вы можете не заметить симптомы этого заболевания, так как зачастую они не выражены явно, а в ряде случаев становятся заметными уже осложнения. Однако если кардиомиопатия сердца уже проявила себя, не заметить ее сложно.
- При сильной физической нагрузке вы чувствуете одышку и нехватку воздуха.
- Появляется длительная ноющая боль в груди.
- Заметны слабость, головокружение.
- Постоянные отеки ног, расстройства сна, частые предобморочные состояния.
Эти симптомы говорят о нарушениях сокращения сердца и проблемах с его кровоснабжением. Немедленно обращайтесь к кардиологу при первых их появлениях!
Причины
Существует три группы основных причин развития первичной кардиомиопатии: врожденная, смешанная, и приобретенная. К вторичным относятся кардиомиопатии вследствие какого-либо заболевания.
Врождённая патология сердца развивается вследствие нарушения закладки тканей миокарда во время эмбриогенеза. Причин очень много, начиная от вредных привычек будущей матери и заканчивая стрессами и неправильным питанием. Так же известны кардиомиопатии беременных и воспалительные кардиомиопатии, которые по существу можно назвать миокардитом.
К вторичным формам относятся следующие виды:
- Кардиомиопатия накопленная или инфильтративная. Для нее характерно накопление между клетками или в клетках патологических включений.
- Токсическая кардиомиопатия.
- Эндокринная кардиомиопатия (метаболическая кардиомиопатия, дисметаболическая кардиомиопатия) возникает вследствие нарушения обмена веществ в сердечной мышце.
- Алиментарная кардиомиопатия образуется в результате нарушения питания, а в частности при длительных диетах с ограничением мясных продуктов или голодании.
Проявления ГКМП многообразны и зависят от ряда факторов: степени гипертрофии миокарда, наличия и величины градиента давления, недостаточности митрального клапана, нередко встречающейся у больных, степени уменьшения полости левого желудочка и тяжести нарушения насосной и диастолической функций сердца и др. Жалобы часто отсутствуют.
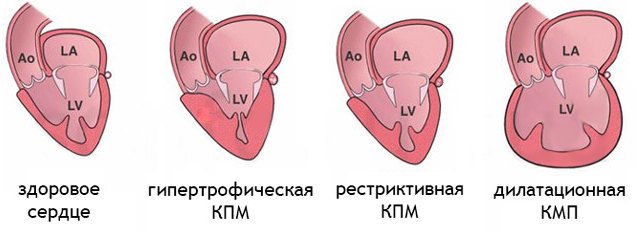
Различают 3 группы КМП:
Гипертрофическую.
Дилатационную (застойную).
Рестриктивную.
Симптомы дилатационной кардиомиопатии:
- Нарастающая сердечная недостаточность.
- Одышка при физической нагрузке.
- Быстрая утомляемость.
- Отеки на ногах.
- Бледность кожи.
- Посинение кончиков пальцев.
Симптомы гипертрофической кардиомиопатии:
- Одышка.
- Боли в грудной клетке.
- Склонность к обморокам, сердцебиению.
Симптомы рестриктивной кардиомиопатии:
- Отеки.
- Одышка.
Основным инструментальным методом диагностики всех видов кардиомиопатий является УЗИ сердца.
Суточное холтеровское мониторирование электрокардиограммы позволяет оценить частоту и выраженность нарушений ритма сердца и внутрисердечных блокад, а так же эффективность проводимого лечения. Лабораторная диагностика важна для контроля эффективности проводимой терапии в оценке состояния водно-солевого баланса, для исключения некоторых побочных эффектов препаратов, а также для выявления вторичных причин поражения сердца.
Лечение
Специфического лечения заболевания не существует.
Вторичная дилатационная кардиомиопатия требует:
- отмены алкоголя при наличии алкогольной зависимости;
- лечения системных заболеваний соединительной ткани и эндокринной системы.
Поскольку эффективное воздействие на причины развития дилатационной кардиомиопатии требует установленной этиологии заболевания, лечение в основном сосредоточено на устранении хронической сердечной недостаточности, которая развивается при ДКМП. Консервативное лечение включает:
- Диету, ограничивающую употребление соли и жидкости.
- Физические нагрузки, которые подбираются индивидуально.
- Употребление ингибиторов АПФ (ангиотензин-превращающего фермента), которые поддерживают в норме АД, уменьшают повреждение мышцы сердца, снижают скорость образования в сердце рубцовой ткани. Дозировка подбирается в индивидуальном порядке.
- Употребление антагонистов рецепторов к ангиотензину. Эта группа препаратов обеспечивает более полную блокировку фермента, превращающего ангиотензин. Обычно назначается при непереносимости ингибиторов АПФ, но возможно и комбинированное лечение этими препаратами.
- Применение бета-адреноблокаторов, которые контролируют ритм сердца и АД. Назначаются обычно совместно с ингибиторами АПФ при наличии у пациента учащенного сердцебиения.
- Употребление антагонистов рецепторов к альдостерону. Эти препараты обладают слабым мочегонным действием и задерживают в организме калий. Назначаются обычно при выраженной сердечной недостаточности.
- Применение диуретиков. Эти мочегонные препараты, удаляющие избыток солей и жидкости из организма, назначаются пациентам, которые страдают задержкой жидкости в организме.
При мерцательной аритмии, которая сочетается с пониженной сократительной способностью сердца, назначаются сердечные гликозиды.
Для лечения и профилактики отрыва кровяных сгустков от места их образования и последующего закрытия этими сгустками сосуда (тромбоэмболия) используются:
- Дезагреганты, которые нарушают склеивание тромбоцитов и замедляют свертываемость крови. Назначаются всем больным с дилатационной кардиомиопатией, если нет противопоказаний.
- Антикоагулянты, которые предотвращают образование новых кровяных сгустков (тромбов). Назначаются при мерцательной аритмии или наличии тромбов в полости сердца.
- Тромболитические средства, которые растворяют имеющиеся тромбы.
При желудочковых аритмиях назначаются антиаритмические средства.
Для лечения дилатационной кардиомиопатии используются также хирургические методы, которые включают:
- Ресинхронизирующую терапию, направленную на восстановление нарушенной внутрисердечной проводимости путем имплантации трехкамерного электростимулятора. Размещенные в желудочках и правом предсердии электроды образуют электрические импульсы, которые передаются сердцу. Данный метод улучшает сердечный кровоток и предупреждают развитие тяжелых осложнений у больных, страдающих неодновременным сокращением желудочков или их мышечных пучков.
- Динамическую кардиомиопластику, которая заключается в оборачивании сердца частью широчайшей мышцы спины. Улучшает способность переносить физическую нагрузку и снижает потребность в приеме лекарств, но на срок жизни влияет не существенно.
- Имплантацию внесердечного (экстракардиального) каркаса, который является сетью, состоящей из скрученных и расположенных слоями нитей. Каркас располагается на границе желудочков и предсердий. Форма и размер имплантата подбираются в индивидуальном порядке при помощи специально изготовленного пластикового макета. Объем максимально растянутого каркаса должен соответствовать максимальному объему сердца в его расслабленном состоянии. Благодаря эластичности сетки обеспечивается постепенное уменьшение объема желудочков. Процедура безопасна, но в настоящее время достаточное количество данных о ее отдаленных последствиях отсутствует.
- Трансплантацию (пересадку) сердца. Эта операция значительно удлиняет срок жизни, но используется относительно редко из-за нехватки донорских сердец и высокой стоимости операции.
- Имплантацию насосов, которые вживляются в области верхушки левого желудочка сердца. Эти устройства механической поддержки, перекачивая кровь в аорту, удлиняют срок жизни и увеличивают переносимость нагрузок. При этой операции существует риск развития инфекционных осложнений, тромбозов и тромбоэмболии.
Тяжелая недостаточность клапанов устраняется путем их протезирования.
Классификации кардиомиопатий
Классификация кардиомиопатий по происхождению
По происхождению различают первичную (заболевания миокарда неясного генеза) и вторичную кардиомиопатию (причина поражения миокарда известна или связана с заболеваниями других органов).
Причины первичной кардиомиопатии:
- Генетические нарушения;
- вирусные инфекции (Коксаки и др.);
- замещение сердечной мышцы соединительной или жировой тканью.
Причины вторичной кардиомиопатии:
- эндокринные нарушения (тиреотоксикоз, сахарный диабет);
- интоксикации (токсическая, алкогольная и др.);
- стресс (кардиомиопатия такоцубо).
Классификация кардиомиопатии по клиническим признакам (основные формы):
Дилатационная кардиомиопатия — наиболее тяжелая и распространенная. При этом заболевании имеет место кардиомегалия — значительное увеличение полостей миокарда. В результате сердце теряет способность полноценно перекачивать кровь. Дилатационная КМП неизбежно приводит к развитию сердечной недостаточности.
Перипартальная (послеродовая) кардиомиопатия — одна из разновидностей дилатационной кардиомиопатии. Как ни парадоксально, развитие у женщины сердечной недостаточности и характерных для нее симптомов — практически основной признак перипартальной формы. Среди других распространенных вариантов — алкогольная.
Гипертрофическая кардиомиопатия (ГКМП) — одна из главных причин внезапной смерти у молодых, физически активных людей (спортсменов, военнослужащих). Эта кардиомиопатия связана с утолщением миокарда (гипертрофия сердечной мышцы). Рост толщины стенки опережает развитие сосудов и как следствие-нарушается кровоснабжение мышцы сердца, также страдает наполнение желудочков кровью.
ГКМП чаще встречается у мужчин.
Обструктивная кардиомиопатия (субаортальный подклапанный стеноз) -разновидность гипертрофической кардиомиопатии, при которой ограничен кровоток, проходящий в аорту из левого желудочка, локально утолщенной межжелудочковой перегородкой.
Рестриктивная кардимиопатия — редкая патология, при которой ухудшаются эластичные свойства сердечных стенок. Миокард теряет способность к растяжению и расслаблению, что нарушает его способность наполняться кровью. Итогом становится застой крови в венах и нехватка ее в артериях. Вероятная причина этого — аномальное разрастание соединительной ткани.
Аритмогенная правожелудочковая кардиомиопатия (болезнь Фонтана) — сопровождающаяся жизнеугрожающими аритмиями.
Аритмогенная КМП может стать причиной желудочковой аритмии у детей и молодых людей с внешне неизмененным сердцем, а также у более взрослых пациентов. Исходом этого заболевания часто является внезапная смерть, особенно в молодом возрасте.
Кардиомиопатия такоцубо (синдром разбитого сердца) — весьма редкое заболевание, при котором развивается внезапное преходящее снижение сократимости миокарда. Форма левого желудочка из-за патологического расширения внешне уподобляется такоцубо — ловушке для осьминогов в Японии (именно в этой стране данный синдром был обнаружен и описан).
КМП такоцубо является причиной острой сердечной недостаточности. Чаще выявляется у женщин в постменопаузе, развивается на фоне тяжелого психоэмоционального потрясения. На ЭКГ может маскироваться под инфаркт миокарда.
1
Анализы при кардиомиопатиях
2
Диагностика кардиомиопатии
3
ЭКГ при кардиомиопатиях
Рекомендации
Диета
Употребление большого количества жидкости имеет очень важное значение. Выпивайте по крайней мере от 6 до 8 стаканов воды в день
В жаркую погоду, следует увеличить потребление жидкости. Жидкость и ограничения в употреблении соли, необходимы для пациентов с сердечной недостаточностью. Посоветуйтесь с вашим лечащим врачом о принципах воздействия на ваш организм конкретных жидкостей и диетических напитков, включая информацию о воздействии алкоголя и кофеина.
Физические упражнения
Ваш врач подскажет, рекомендуется ли вам заниматься спортом или нет. Большинству людей с кардиомиопатией предлагаются легкие занятия аэробикой. Тем не менее, ваш врач, основываясь на симптомах и тяжести вашей болезни, может попросить вас воздержаться от каких либо физических нагрузок. Так же, как и при дилатационной кардиомиопатии, не рекомендуется поднятие тяжестей
Регулярное посещение врача
Пациенты с ГКМП минимум раз в год должны посещать врача кардиолога и контролировать свое состояние. Посещения врача могут быть более частыми, в том случае, когда гипертрофическая кардиомиопатия была диагностирована впервые.
Атрезия легочной артерии с дефектом межжелудочковой перегородки
Порок включает 5 компонентов (рис.117):
- атрезию легочного ствола;
- окклюзию выводного отдела правого желудочка;
- большой ДМЖП;
- декстрапозицию корня аорты;
- какой-либо источник коллатерального кровоснабжения легких
(ОАП, аортолегочные коллатеральные артерии).
Рис.117.
Атрезия легочной
артерии.
Дефект
межжелудочковой
перегородки.
Открытый
артериальный проток.
Данный вариант порока нередко определяется как крайняя
форма тетрады Фалло.
ЭхоКГ критерии
Одномерная ЭхоКГ:
- Отсутствие переднего продолжения.
- Перерыв эхосигнала от межжелудочковой перегородки
при М-сканировании от верхушки к основанию сердца. - Дилатация аорты.
- Декстрапозиция аорты.
- Невозможность визуализации клапана легочной артерии.
- Гипертрофия межжелудочковой перегородки.
- Гипертрофия передней стенки правого желудочка.
- Нормальный или уменьшенный (в 40%) размер левого
желудочка.
Двухмерная ЭхоКГ:
- Непосредственная визуализация большого ДМЖП обычно
в подаортальной зоне. - Невозможность визуализации ствола легочной артерии
или резкая его гипоплазия. - Декстрапозиция аорты.
- Выявление сопутствующих врожденных аномалий (ОАП,
ДМПП, аномальный дренаж легочных вен).
Допплер-ЭхоКГ:
- Турбулентный поток через дефект межжелудочковой
перегородки с определением градиента давления в правом желудочке. - Выявление сопутствующих врожденных аномалий.
- Общий артериальный ствол.
- Тетрада Фалло.
Правое предсердие
Функциональная анатомия правого предсердия
Правое предсердие имеет цилиндрическую форму; у новорожденных объем
полости составляет 6,5-10 см3, к концу 1 года жизни — 11-18
см3, в 7-9 лет — 22-36 см3, в 18-25 лет — 100-150
см3.
Правое предсердие изучают в двухмерном режиме из проекции 4-х камер
с верхушки или субксифоидально. При субксифоидальном доступе можно
визуализировать место впадения нижней полой вены, а также ее заслонку
(складка эндокарда высотой 5-10 мм) и межвенозный бугорок (на границе
устьев верхней и нижней полой вены). На латеральной стенке правого
предсердия в ряде случаев удается визуализировать мышечный валик (пограничный
гребень ушка правого предсердия). При дилатации ушка могут визуализироваться
гребенчатые мышцы в виде трабекулярных образований, обычно соединяющихся
с устьем полых вен.
Размеры правого предсердия зависят от возраста: у новорожденных и
детей до года переднезадний размер колеблется от 1,1 до 2,1 см, у
детей 1-6 лет — 1,1-2,5 см, у детей 7-12 лет — 1,3-2,5 см, 13-17
лет — 1,4-2,5 см. Ширина предсердия у новорожденных и детей до 1
года от 1,2 до 1,9 см, у детей 1-6 лет — 1,2-2,3 см, у детей 7-12
лет — 1,3-2,3 см, у 13-17-летних — 1,4-2,3 см.
Двухмерная эхокардиография правого предсердия
Правое предсердие визуализируют в нескольких продольных и поперечных
сечениях. Из субкостального доступа определяют место впадения нижней
полой вены в полость камеры (situs solitus). В проекции 4-х камер
из апикального или субкостального доступа устанавливают форму камеры,
наличие в ней дополнительных образований, взаимосвязь с желудочковой
камерой.
Дилатация правого предсердия
- Идиопатическая аневризма правого предсердия.
- Аномальный дренаж легочных вен.
- Дефект межпредсердной перегородки.
- Открытый атриовентрикулярный канал.
- Аномалия Эбштейна.
- Стеноз трикуспидального клапана.
- Недостаточность трикуспидального клапана.
- Опухоль правого предсердия.
- Рестриктивная кардиомиопатия.
- Аритмогенная дисплазия правого желудочка.
- Частичное врожденное отсутствие перикарда.
- Легочное сердце.
- Застойная сердечная недостаточность.
- Констриктивный перикардит.
- Прорыв аневризмы синуса Вальсальвы в правое предсердие.
- Портальная гипертензия.
Уменьшение полости правого предсердия
- Сдавление при опухолях средостения.
- Синдром гипоплазии правого желудочка.
- Большой лево-правый шунт на уровне желудочков (ДМЖП)
или магистральных сосудов (ОАП).
Дополнительные эхосигналы в полости правого предсердия:
- Опухоли правого предсердия (чаще миксомы).
- Заслонка венечного синуса.
- Заслонка нижней полой вены (Евстахиев клапан).
- Заслонка овального отверстия.
- Гребенчатые мышцы ушка правого предсердия.
- Тромб в правом предсердии.
- Пролапс трикуспидального клапана.
- Пролапс клапана нижней полой вены.
- Аневризма межпредсердной перегородки.
Симптомы и причины гипертрофической кардиомиопатии
Человек может страдать гипертрофической кардиомиопатией и никогда не чувствовать никаких симптомов, но имеются возможные симптомы, такие как:
- Боль в груди при стрессе, известная как стенокардия;
- Учащенное сердцебиение;
- Сбивчивое дыхание;
- Чувство слабости.
Симптомы могут появиться на любом этапе жизни человека, от подросткового возраста до среднего возраста или старше.
Точная причина гипертрофической кардиомиопатии неизвестна, но, по-видимому, она является генетической мутацией.
Исследования показывают, что от 50 до 60% людей с гипертрофической кардиомиопатией имеют близких родственников с этим заболеванием.
Генетическая причина гипертрофической кардиомиопатии у людей без семейного анамнеза этого заболевания известна как мутация de novo.
Транспозия магистральных сосудов
При транспозиции аорта находится справа и спереди от легочной артерии
(D-транспозиция) или спереди и слева (L-транспозиция и сообщается
с правым желудочком; легочная артерия находится слева и сзади и сообщается
с левым желудочком. Связь между легочной и системной циркуляцией осуществляется
через ДМЖП, ДМПП, ОАП или большие бронхиальные артерии (рис.119).
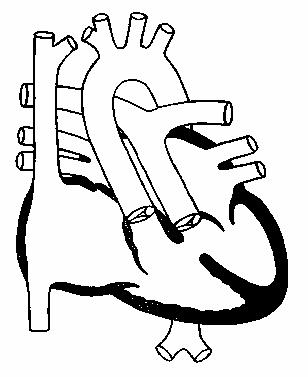
Рис.119.
Транспозиция
магистральных
сосудов (схема).
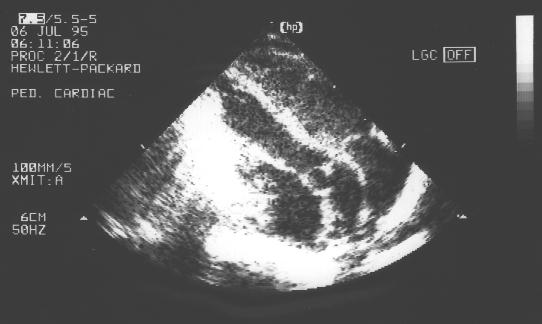
Рис.120.
Транспозиция
магистральных
сосудов в двухмерном
режиме.
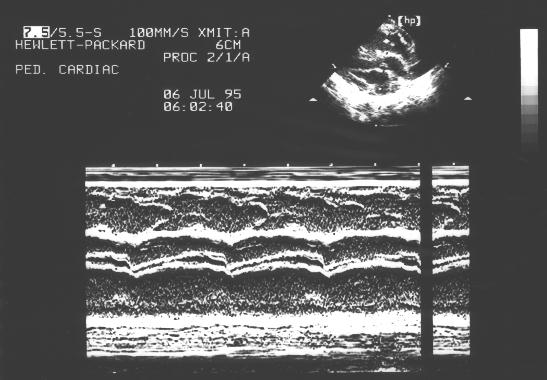
Рис.121.
Транспозиция
магистральных
сосудов в одномерном
режиме.
ЭхоКГ критерии
Одномерная ЭхоКГ:
- Одновременная запись двух полулунных клапанов,при
этом клапан легочной артерии имеет более короткий период изгнания. - Дилатация правого желудочка.
- Гипертрофия правого желудочка.
- Увеличение экскурсии передней створки трикуспидального
клапана.
Двухмерная эхоКГ:
- Идентификация спереди и справа (D-транспозиция)
или спереди и слева (L-транспозиция) аорты и сзади легочной артерии.
Эти сосуды лежат один под другим. Легочная артерия лежит кзади и можно
видеть ее бифуркацию. - В продольном сечении видна параллельная ориентация
выводных трактов обоих желудочков и обоих магистральных сосудов, при
этом легочная артерия не огибает аорту. - Легочная артерия отходит от левого желудочка и формирует
митрально-полулунное продолжение. - Аорта отходит от правого желудочка.
- Выявление сопутствующих внутрисердечных аномалий:
большой дефект межжелудочковой перегородки, открытый артериальный
проток, общий атриовентрикулярный канал, стеноз или атрезия легочной
артерии, гипоплазия (атрезия) атриовентрикулярного клапана.
- Турбулентный поток крови через дефект межжелудочковой
перегородки. - Оценка степени легочного кровотока (ТМС с усиленным
легочным кровотоком, ТМС с ослабленным легочным кровотоком). - Выявление сопутствующих врожденных аномалий.
Лечение гипертрофической кардиомиопатии
Для лечения применяют препараты, обладающие отрицательным инотропным эффектом:
- бета-адреноблокаторы — неселективные («Пропранолол»), селективные («Метапролол», «Бисопролол»). В настоящий момент предпочтение отдают применению селективных β-блокаторов;
- блокаторы кальциевых каналов («Верапамил»);
- «Дизопирамид».
При фибрилляции предсердий показаны антикоагулянты.
Возможно хирургическое лечение, показаниями для которого являются выраженная гипертрофия левого желудочка и неэффективность медикаментозной терапии. Основным методом оперативного лечения является миэктомия по Морроу: резекция гипертрофированной части межжелудочковой перегородки, что приводит к нормализации гемодинамики и уменьшению клинических проявлений заболевания.
Основные лекарственные препараты
Имеются противопоказания. Необходима консультация специалиста.
- Метопролол (антиаритмическое, гипотензивное, антиангинальное средство). Режим дозирования: внутрь, во время или сразу после еды, не разжевывая и запивая жидкостью, по 100 мг утром и вечером.
- Дизопирамид (антиаритмическое средство). Режим дозирования: внутрь, в суточной дозе 600 мг, разделенной на 4 приема.
- Кордарон (антиангинальное, коронарорасширяющее, антиаритмическое средство). Режим дозирования: внутрь, в начальной дозе 600-800 мг/сут., разделенной на несколько приемов, до достижения суммарной дозы 10 г. Поддерживающая доза 100-400 мг/сут., ее можно принимать через день или делать перерывы в приеме 2 дня в неделю.
Диагностика гипертрофической кардиомиопатии
- Электрокардиография: признаки гипертрофии левого желудочка.
- Эхокардиография: позволяет определить степень гипертрофии миокарда, оценить состояние систолической и диастолической функции миокарда, размеры полости левого желудочка.
- Рентгенография органов грудной клетки.
- Эндомиокардиальная биопсия: применяется при недостаточной информативности клинических и инструментальных данных.
- Генетическое исследование: выявляет характерные мутации генов контролирующих синтез сократительных белков миокарда.
Наиболее информативным является эхокардиографическое исследование.
Вторичные кардиомиопатии сердца
В эту группу объединены патологии, причины возникновения которых кроются в физических и химических нарушениях в организме, провоцирующих изменения в сердечной мышце.
-
Алкогольная кардиомиопатия является следствием воздействия на миокард этанола, составляющего основу спиртных напитков. В итоге в миокарде появляется жировая ткань.
-
Тиреотоксическая вызывается нарушением функции эндокринной системы, отсутствием лечения при тиреотоксикозе. Одно из частых проявлений – дисгормональная кардиомиопатия в период полового созревания или при гормональной терапии.
-
Токсическая — ещё один вид вторичной кардиомиопатии, связанный с воздействием на ткани сердца различных ядовитых веществ: лития, кобальта и др. Они вызывают воспаления и микроинфаркты.
-
Стрессовая сопровождается снижением сокращений миокарда и его слабостью вследствие эмоциональных, психических воздействий, потрясений.
-
Диабетическая появляется при диагнозе «сахарный диабет» и ведет к биохимическим изменениями в миокарде, накоплению различных полисахаридов.
Прогнозы при каждом виде вторичной кардиомиопатии зависят от успешности лечения не только самой патологии, но и заболеваний, ставших ее причиной: сахарного диабета, тиреотоксикоза, алкогольной зависимости и др. Это чрезвычайно сложные случаи, однако при профессиональном подходе длительность жизни пациента может быть максимально увеличена.
Лечение дилатационной кардиомиопатии
Лечение ДКМП — это лечение хронической сердечной недостаточности (ХСН) в чистом виде, поскольку этиотропное лечение возможно лишь при известной этиологии ДКМП
Еще одной важной целью является уменьшение размеров сердца, для этого должен быть снижен уровень гормонов в крови, которые приводят к его увеличению и, в конечном счете, к ухудшению симптомов. Пациенты обычно принимают различные лекарства для лечения сердечной недостаточности. Врачи кардиологи также рекомендуют изменения в образе жизни
Какие препараты используются для лечения ДКМП?
Для улучшения работы сердца, большинство людей, принимают такие лекарства, как бета-блокаторы, ингибиторы АПФ и/или различные мочегонные средства. Если у вас аритмия, врач может дать вам лекарство для контроля сердечного ритма. Растворители крови могут быть использованы, чтобы предотвратить образование кровяных сгустков. Обсудите с вашим врачом, какое лечение вам больше подходит.
Что используют в хирургии для лечения ДКМП?
Людям с тяжелой формой дилатационной кардиомиопатии, возможно, потребуется одна из следующих операций:
- Сердечная ресинхронизирующая терапия — трёхкамерная стимуляция сердца (один электрод в правом предсердии, два — в желудочках).
- Операция окутывания сердца эластичным сетчатым каркасом — предотвращает прогрессирование ХСН, на начальных стадиях ДКМП может привести к обратному развитию заболевания.
- Механические желудочки сердца (микронасос, установленный в полости левого желудочка) — могут использоваться для временной поддержки гемодинамики, но показано, что через несколько месяцев работы аппарата улучшаются функции самого сердца.
- Трансплантация сердца — в настоящее время уже не считается средством выбора в лечении ДКМП, ввиду возможности альтернативных процедур, перечисленных выше.
Прогноз при ДКМП остается крайне серьезным — в случае идиопатической формы заболевания ежегодная летальность от 5 до 45%, для форм с известной этиологией смертность может быть меньше. Успехи в лечении привели к существенному увеличению выживаемости при этой форме кардиомиопатии.