Геморрагический васкулит
Содержание:
Лечение Геморрагического васкулита:
Лечение больных геморрагическим васкулитом — сложная задача; не существует лекарственных препаратов, эффективно подавляющих основной патологический процесс независимо от его локализации. Необходимо исключить воздействие заведомо активных антигенных воздействий, особенно тех, которые хронологически совпадали с клиническими проявлениями болезни. В активную фазу болезни следует избегать контрастных температурных влияний, продолжительного стояния и длительной ходьбы, так как при этом могут заметно усилиться кожные кровоизлияния (прежде всего на ногах). Применение кортикостероидов (начиная с 20-40 мг преднизолона в день) считается наиболее эффективным при выраженных артритах и, судя по некоторым сообщениям, при желудочно-кишечных кровотечениях, вызванных геморрагическим васкулитом. Влияние на кожные высыпания и поражение почек менее отчетливое, хотя у ряда больных соответствующие клинико—лабораторные проявления под влиянием гормональной терапии могут несколько уменьшаться.
Мы наблюдали положительное влияние при различных локализациях болезни (особенно при преимущественно кожном варианте) продектина, назначаемого по 0,75-1,5 г/сут в течение 2-3 мес. Продектин может сочетаться с любыми Препаратами, используемыми в терапии геморрагического васкулита. Поскольку артрит при этом заболевании, как правило, бывает нетяжелым, мы предпочитаем использовать для лечения в качестве препаратов «первого ряда» НПВП, в первую очередь вольтарен (150- 100 мг/сут). При рецидивирующем течении заболевания в лечебный комплекс следует включать длительный прием плаквенила по 0,2 г в день или делагила (по 0,25 г). При стойком и тем более прогрессирующем поражении почек вместо делагила и плаквенила целесообразно использовать иммунодепрессанты типа азатиоприна. В подобных случаях отмечен также положительный лечебный эффект плазмафереза.
Болезни — враги вашего малыша
Непрекращающиеся болезни кардинальным образом нарушают у детей нормальный темп жизни и развития, подрывая как физическое, так и психическое здоровье:
Болезни наносят вред организму ребенка. У маленького человека, который часто болеет, формируется порочный круг: на фоне ослабленного иммунитета он заболевает ОРЗ, что, в свою очередь, еще больше ослабляет его иммунитет. В результате организм малыша становится очень чувствительным к различным инфекционным агентам, снижаются естественные механизмы защиты. Это приводит к развитию различных хронических вялотекущих инфекционных и неинфекционных заболеваний (хронический гайморит, фронтит, гастрит и язвенная болезнь желудка и двенадцатиперстной кишки, бронхиальная астма и так далее). Хронические инфекции приводят к отставанию ребенка в физическом развитии, повышенной аллергизации.
Формируют невротический тип личности. У ребенка, который постоянно болеет, формируется определенное представление о себе как о слабом, беззащитном, неудачливом. Такие дети растут замкнутыми, неуверенными в себе, тревожными. Кроме того, очень часто у такого ребенка развиваются ипохондрические черты личности: он склонен к чрезмерной фиксации на своем теле, болезнях, любит о них рассказывать, ходить к врачам и жаловаться на свое здоровье
В глубине души эти люди уверены, что только таким способом они могут привлечь внимание окружающих, вызвать к себе симпатию, уважение, сочувствие. Также очень часто у болеющих детей развивается опасный психологический механизм защиты — соматизация проблем
На любые негативные переживания, нерешенные конфликты, стрессы они реагируют одним известным им способом — болезнью. Таков механизм формирования психосоматических заболеваний, которые сложно поддаются лечению.
Мешают занять свое место в жизни. Ребенку, который часто болеет, приходится пропускать детский сад и занятия в школе. Это приводит к тому, что у малыша будет меньше знаний и навыков, чем у его более здоровых сверстников, ему тяжелее будет усвоить новую информацию. Именно поэтому такие дети часто отстают в учебе, у них нет или очень мало увлечений. Кроме того, частое отсутствие в школе и детском саду значительно нарушает социальную адаптацию ребенка: болеющим детям всегда очень сложно освоиться в детском коллективе, другие их часто обижают, считая слабыми. Сам ребенок также себя воспринимает как менее успешного и способного, чем другие ребята. Такие дети боятся проявлять себя, не стремятся к успеху, чувствуют себя отвергнутыми в коллективе.
Гранулематоз Вегенера (Wegener)
Патология известна также как злокачественная гранулема, — некротизирующий гранулематозный васкулит мелких сосудов с поражением дыхательных путей, почек, кожи и других органов и тканей
Механизм этого редкого заболевания неизвестен. Развитию патологии способствует микробный фактор (герпесвирусы, Staphylococcus aureus и др.). У большинства больных гранулематозом Вегенера имеются антитела против протеиназы-3 DR3) азурофильных гранул нейтрофилов, обозначаемые ANCA антинейтрофильные цитоплазматические антитела). Эти антитела распределяются диффузно в цитоплазме нейтрофилов. При активации клеток этот фермент (PR3) экспрессируется на мембране.
Кроме того у больных обнаружены антитела против других компонентов нейтрофилов, миелопероксидазы, эластазы, лизоцима и лактоферрина. Антитела против РРЗ, связанные с нейтрофилами, стимулируют их к выбросу активированных радикалов кислорода, перекиси водорода и ферментов, разрушающих стенки сосудов. Эти активированные субстанции повреждают базальную мембрану клубочков почки. Развиваются клеточные инфильтраты, гранулемы, гиалиноз и склероз сосудистых стенок.
Симптомы (проявления)
Клиническая картина характеризуется общими признаками для разных васкулитов. Отмечаются синусит, ринит, воспаление среднего уха, бронхит, пневмония, каверны в легких, поражения органов зрения и почек (очаговый нефрит, некротизирующийся гломерулонефрит), эрозии, инфаркты и некрозы внутренних органов. Возникают язвы слизистой оболочки рта. Развиваются слабость, ночные поты и лихорадка. Для половины больных характерны кожные изменения: пальпируемая пурпура, язвенно-некротические очаги, гранулемы. Появляются мышечные и суставные боли. Снижается масса тела. Происходит чередование обострений и ремиссий. Обострение отмечается в холодный период года. Большинство больных погибает в течение 2 лет.
Лабораторная диагностика
Отмечается ускорение СОЭ и повышение содержания С-реактивного белка в сыворотке крови. Развиваются лейкоцитоз, тромбоцитоз, анемия. При серологическом исследовании в сыворотке крови обнаруживают антитела АКІСА (цитоплазматические АЫСА против РБЗ).
Лечение
Лечение одинаковое для системных васкулитов. Назначают ангиопротекторы, кортикостероиды и иммунодепрессанты (циклофосфамид и др.).
Online-консультации врачей
| Консультация офтальмолога (окулиста) |
| Консультация неонатолога |
| Консультация андролога-уролога |
| Консультация радиолога (диагностика МРТ, КТ) |
| Консультация анестезиолога |
| Консультация психолога |
| Консультация психиатра |
| Консультация пластического хирурга |
| Консультация эндокринолога |
| Консультация гастроэнтеролога детского |
| Консультация невролога |
| Консультация маммолога |
| Консультация специалиста банка пуповинной крови |
| Консультация генетика |
| Консультация онколога-маммолога |
Новости медицины
Футбольные фанаты находятся в смертельной опасности,
31.01.2020
«Умная перчатка» возвращает силу хвата жертвам травм и инсультов,
28.01.2020
Назван легкий способ укрепить здоровье,
20.01.2020
Топ-5 салонов массажа в Киеве по версии Покупон,
15.01.2020
Новости здравоохранения
Глава ВОЗ объявил пандемию COVID-19,
12.03.2020
Коронавирус атаковал уже более 100 стран, заразились почти 120 000 человек,
11.03.2020
Коронавирус атаковал 79 стран, число жертв приближается к 3200 человек,
04.03.2020
Новый коронавирус атаковал 48 стран мира, число жертв растет,
27.02.2020
Анализ на С-реактивный белок
С-реактивный белок (СРБ) – очень чувствительный элемент анализа крови, который быстро реагирует даже на мельчайшее повреждение ткани организма. Присутствие С-реактивного белка в крови является предвестником воспаления, травмы, проникновения в организм бактерий, грибков, паразитов.
СРБ точнее показывает воспалительный процесс в организме, чем СОЭ (скорость оседания эритроцитов). В то же время С-реактивный белок быстро появляется и исчезает – быстрее, чем изменяется СОЭ.
За способность С-реактивного белка в крови появляться в самый пик заболевания его еще называют «белком острой фазы».
При переходе болезни в хроническую фазу С-реактивный белок снижается в крови, а при обострении процесса повышается вновь.
С-реактивный белок норма
С-реактивный белок производится клетками печени и в сыворотке крови содержится в минимальном количестве. Содержание СРБ в сыворотке крови не зависит от гормонов, беременности, пола, возраста.
Норма С-реактивного белка у взрослых и детей одинаковая – меньше 5 мг/ л (или 0,5 мг/ дл).
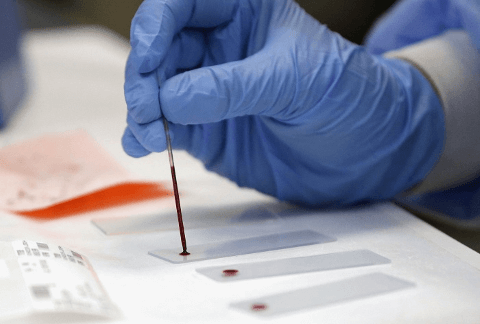
Анализ крови на С-реактивный белок берется из вены утром, натощак.
1
Анализ крови на уровень мочевой кислоты
2
анализ крови на антинуклеарные антитела
3
Исследование крови на ревматоидный фактор
Причины повышения С-реактивного белка
С-реактивный белок может быть повышен при наличии следующих заболеваний:
- ревматизм;
- острые бактериальные, грибковые, паразитарные и вирусные инфекции;
- желудочно-кишечные заболевания;
- очаговые инфекции (например, хронический тонзиллит);
- сепсис;
- ожоги;
- послеоперационные осложнения;
- инфаркт миокарда;
- бронхиальная астма с воспалением органов дыхания;
- осложненный острый панкреатит;
- менингит;
- туберкулез;
- опухоли с метастазами;
- некоторые аутоиммунные заболевания (ревматоидный артрит, системный васкулит и др.).
При малейшем воспалении в первые же 6-8 часов концентрация С-реактивного белка в крови повышается в десятки раз. Имеется прямая зависимость между тяжестью заболевания и изменением уровня СРБ. Т.е. чем выше концентрация С-реактивного белка, тем сильнее развивается воспалительный процесс.
Поэтому изменение концентрации С-реактивного белка используется для мониторинга и контроля эффективности лечения бактериальных и вирусных инфекций.
Разные причины приводят к разному повышению уровня С-реактивного белка:
- Наличие бактериальных инфекций хронического характера и некоторых системных ревматических заболеваний повышает С-реактивный белок до 10-30 мг/л. При вирусной инфекции (если нет травмы) уровень СРБ повышается незначительно. Поэтому высокие его значения указывают на наличие бактериальной инфекции.
- При подозрении на сепсис новорожденных уровень СРБ 12 мг/л и более говорит о необходимости срочной противомикробной терапии.
- При острых бактериальных инфекциях, обострении некоторых хронических заболеваний, остром инфаркте миокарда и после хирургических операциях самый высокий уровень СРБ – от 40 до 100 мг/л. При правильном лечении концентрация С-реактивного белка снижается уже в ближайшие дни, а если этого не произошло, необходимо обсудить другое антибактериальное лечение. Если за 4-6 дней лечения значение СРБ не уменьшилось, а осталось прежним и даже увеличилось, это указывает на появление осложнений (пневмония, тромбофлебит, раневой абсцесс и др.). После операции СРБ будет тем выше, чем тяжелее была операция.
- При инфаркте миокарда белок повышается через 18-36 часов после начала заболевания, через 18-20 дней снижается и к 30-40 дню приходит к норме. При стенокардии он остается в норме.
- При различных опухолях повышение уровня С-реактивного белка может служить тестом для оценки прогрессирования опухолей и рецидива заболевания.
- Тяжелые общие инфекции, ожоги, сепсис повышают С-реактивный белок до огромнейших значений: до 300 мг/л и более.
- При правильном лечении уровень С-реактивного белка снижается уже на 6-10 день.
Подготовка к ревматологическим анализам
Чтобы анализы показывали объективную информацию, необходимо придерживаться некоторых правил. Сдавать кровь нужно в утренние часы, натощак. Между взятием анализов и приемом пищи должно пройти приблизительно 12 часов. Если мучает жажда, выпейте немного воды, но не сок, чай или кофе. Необходимо исключить интенсивные физические упражнения, стрессы. Нельзя курить и употреблять спиртное.
Диагностика
Так как заболевание имеет несколько разновидностей, определить тип сложно только при осмотре пациента. Если есть подозрение на наличие аллергического васкулита, лечение назначают после проведения ряда диагностических методик:
- Анализ крови проводится всем пациентам независимо от возраста. Здесь можно выявить, сколько лейкоцитов присутствует, как движутся эритроциты. При исследовании сыворотки крови врач увидит количество иммуноглобулинов.
- Биопсия кожи считается одной из главных методик при диагностировании аллергического васкулита. Для этого небольшую частичку кожи больного оправляют на исследование. На основании проб выявляют, какие изменения происходят на коже.
- Иммунологическое обследование необходимо для того, чтобы обнаружить антитела и иммунные клетки, влияющие на развитие заболевания. Для этого понадобится забор крови из вены.
- Понадобится кардиограмма и рентген внутренних органов, проведение ангиографии артерий.
При общем обследовании можно выявить хронических возбудителей, имеются ли осложнения в печени, суставах и артериях, провоцирует ли болезнь какая-нибудь инфекция. Общую программу подбирает специалист в индивидуальном порядке.
Осуществляется диагностика в больнице опытным врачом. Обычно поставить диагноз удается уже при первом посещении, но врач может назначить дополнительные исследования:
- Биопсия кожи.
- Анализ крови, мочи.
- Биохимические пробы печени.
- Определение АСЛ-О и ЦИК.
Для подбора правильного лечения пациента необходимо провести исследования, позволяющие выявить причину, повлекшую за собой развитие васкулита. К ним относят:
- общий анализ мочи и крови, биохимию;
- ЭКГ;
- УЗИ и рентген внутренних органов (брюшной полости, малого таза);
- анализ крови на антигены и общее состояние иммунитета.
Также обязательно нужны осмотры кардиолога, ревматолога и невропатолога. Чтобы определить степень вовлечения в патологический процесс других органов организма, необходимы консультации пульмонолога, нефролога, гастроэнтеролога, окулиста.
Если заболеванию предшествовали аллергические реакции, надо дополнительно обследоваться у аллерголога.
- общий и биохимический анализ крови;
- иммунограмма;
- общий анализ мочи;
- ультразвуковое исследование внутренних органов;
- ангиографию;
- допплер-исследование;
- магнитно-резонансную или компьютерную томографию;
- электрокардиографию;
- реовазографию;
- электроэнцефалографию.
Узкие специалисты для уточнения диагноза, определения степени поражения организма и тяжести состояния ребенка могут рекомендовать провести и другие обследования и анализы. Это поможет подобрать наиболее эффективное лечение и защитить ребенка от инвалидности.
После тщательного общего осмотра и подробного изучения истории болезни врач назначает нужные заболевшему обследования:
- анализы мочи, крови, биохимия кровяной сыворотки;
- исследование сыворотки крови и определение в ней количества иммуноглобулинов;
- кардиограмма сердца;
- рентген внутренних органов;
- определение общего состояния иммунитета;
- ангиография органов и артерий.
Пациенты с подозрением на аллергический васкулит нуждаются в консультации ревматолога. Из-за выраженного разнообразия проявлений и форм аллергического васкулита его диагностика является сложной задачей для врача.
Из лабораторных методов диагностики при аллергическом васкулите применяются клинический анализ крови и мочи, анализ крови на сахар, биохимические пробы печени, определение АСЛ-О и ЦИК. Гистологическая картина аллергического васкулита характеризуется набуханием и отечностью эндотелия кожных и подкожных сосудов, его разрастанием с сужением просвета пораженного сосуда, лейкоцитарной инфильтрацией сосудистой стенки, отложением в ней геморсидерина, микротромбозами и выходом элементов крови за пределы сосуда.
Проведение РИФ позволяет выявить отложение в стенке пораженного сосуда иммуноглобулинов и комплексов антиген-антитело.
Диагностика сопутствующих сосудистых нарушений может потребовать консультации кардиолога, флеболога или сосудистого хирурга, проведения ЭКГ, ангиографии, УЗДГ артерий и вен.
- анализ крови, мочи;
- определение АСЛ-О;
- анализ на количество иммуноглобулинов крови;
- бактериологическое обследование;
- полимеразная цепная реакция (ПЦР) при инфекциях;
- электрокардиограмма;
- рентгенография;
- УЗИ;
К каким докторам следует обращаться если у Вас Аллергический артериолит, или васкулит Рейтера:
- Дерматолог
- Инфекционист
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Аллергического артериолита, или васкулита Рейтера, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору – клиника Eurolab всегда к Вашим услугам! Лучшие врачи осмотрят Вас, изучат внешние признаки и помогут определить болезнь по симптомам, проконсультируют Вас и окажут необходимую помощь и поставят диагноз. Вы также можете вызвать врача на дом. Клиника Eurolab открыта для Вас круглосуточно.
Как обратиться в клинику:
Телефон нашей клиники в Киеве: (+38 044) 206-20-00 (многоканальный). Секретарь клиники подберет Вам удобный день и час визита к врачу. Наши координаты и схема проезда указаны здесь. Посмотрите детальнее о всех услугах клиники на ее персональной странице.
Лечение
Обязательна госпитализация больных и соблюдение постельного режима в течение первых 2—3 недели заболевания. Из рациона исключают сенсибилизирующие пищевые продукты (цитрусовые, шоколад, свежие ягоды). Следует избегать применения лекарственных препаратов, если прогноз их эффекта сомнителен. Антибиотики назначают только при доказанной бактериальной инфекции. Димедрол, супрастин, тавегил и другие антигистаминные препараты не эффективны, как и широко применявшиеся ранее препараты кальция, аскорбиновая кислота, рутин. Используют нестероидные противовоспалительные препараты (индометацин, вольтарен). Глюкокортикоидные гормоны, но данным И. Е. Тареевой (1983), оказывают в ряде случаев благоприятное действие при кожном и суставном синдромах, но не влияют на патологический процесс в почках; вместе с тем они повышают свертываемость крови, ингибируют фибринолиз, усугубляют внутрисосудистое свертывание крови
Поэтому их назначают с осторожностью и только в комплексе с гепарином. Применение гепарина наиболее эффективно в связи с многосторонним действием препарата на патогенетические факторы Шенлейна—Геноха болезни
Он устраняет гиперкоагуляцию и купирует диссеминированное свертывание крови, ингибирует комплемент и препятствует его дальнейшей активации, стимулирует фибринолиз. Терапию гепарином начинают после определения гепаринорезистентности плазмы in vitro и проводят под контролем показателей свертываемости крови. Обычно гепарин назначают из расчета 300—400 ЕД на 1 кг массы тела в сутки в виде инъекций Под кожу живота (каждые 6—8 часов), при необходимости изменяя дозу так, чтобы обеспечить снижение показателей аутокоагуляционного теста и активированного парциального тромбопластинового времени в 2 раза. При развитии гепарино-резистентности дозу препарата увеличивают (иногда суточную дозу доводят до 800 ЕД на 1 кг массы тела). Если гепаринорезистентность связана с дефицитом антитромбина III, то больным ежедневно вводят в вену струйно 300—400 мл свежезамороженной донорской плазмы. Для улучшения микроциркуляции и усиления фибринолиза рекомендуют внутривенное капельное введение никотиновой кислоты в максимально переносимых дозировках. В качестве дезагреганта может быть использован трентал.
Больным с абдоминальным синдромом назначают полный голод до тех пор, пока не купируются боли. Разрешается только пить воду. При профузном кровотечении из желудочно-кишечного тракта струйно переливают большие дозы свежезамороженной плазмы (до 1000 мл и более). Введение аминокапроновой кислоты противопоказано, так как это может привести к усугублению синдрома диссеминированного внутрисосудистого свертывания. Назначать гепарин и дезагреганты нецелесообразно. При отсутствии эффекта производят резекцию пораженного отдела кишечника.
К наиболее эффективным методам лечения Шенлейна—Геноха болезни относится плазмаферез (см.). Эффект наступает быстро — после первой или второй процедуры. Купируются даже самые тяжелые криоглобулинемические формы васкулитов, протекающие с тяжелым синдромом внутрисосудистого свертывания крови. Обычно проводят 5—6 процедур через 3—4 дня. За сеанс удаляют от 1500 до 2000 мл плазмы больного. Дефицит жидкости и белков восполняют солевыми растворами, реополиглюкином, 10% раствором альбумина, свежезамороженной плазмой. Как при острых, так и при хронических формах Шенлейна—Геноха болезни весьма эффективным оказался так называемый селективный плазмаферез. Суть метода заключается в экстракорпоральном осаждении при t° 4° макромолекулярных агрегатов, в состав которых входят фибронектин, фибриноген, VIII фактор свертывания крови, криоглобулины, иммунные комплексы, обломки клеточных мембран. Перечисленные и другие компоненты плазмы преципитируют в присутствии гепарина. «Очищенная» таким образом плазма может быть заморожена и в дальнейшем перелита больному при следующем гшазмаферезе. При t° —20° пластиковый контейнер с плазмой может храниться в течение недели. При отсутствии эффекта от перечисленных выше методов лечения или при частых и тяжелых рецидивах Шенлейна—Геноха болезни назначают цитостатические препараты, обладающие иммунодепрессивным действием: азатиоприн по 150 мг в сутки в течение 3—4 месяца, циклофосфан по 200 мг через день (суммарная курсовая доза 8—10 г). Лечение цитостатиками нужно проводить под контролем уровня лейкоцитов в крови. Следует избегать использования этих препаратов у детей, учитывая мутагенный эффект цитостатиков.
Патогенез
До сих пор ведется работа над изучением этиологии системного васкулита. В частности, существует мнение о вероятной роли бактериальной или вирусной инфекции в его развитии. Патогенез заболевания комплексный, включающий целый ряд иммунных механизмов. Предполагается, что в развитии системного васкулита играют роль такие факторы:
- Образование в организме аутоантител к антинейтрофильным цитоплазматическим антителам, в процессе которого происходит активация и адгезия нейтрофилов к эндотелиальным клеткам, что ведет к их повреждению.
- Образование аутоантител к антигенам сосудистых стенок.
- Формирование патогенных иммунокомплексов и их депозиция в стенку сосудов. Которые воздействует на полиморфноядерные лейкоциты после активации комплемента. В свою очередь, они продуцируют лизосомальные ферменты, повреждающие сосудистую стенку. Ее проницаемость увеличивается. При иммунном воспалении сосуда часто проявляется тромбоз.
- Реакции иммунной системы, связанные с действием Т-лимфоцитов. Этот механизм является определяющим в развитии гранулематоза Вегенера. Вследствие взаимодействия с антителом сенсибилизированные Т-лимфоциты продуцируют лимфокины, угнетающие миграцию макрофагов. Далее они концентрируют их там, где скапливаются антигены. Макрофаги активируются и продуцируют лизосомальные ферменты, что ведет к повреждению сосудистых стенок. Эти механизмы приводят к проявлению гранулемы.
- Непосредственное влияние разнообразных инфекционных агентов на стенку сосудов.
- Вазоспастические и коагуляционные нарушения.
- Эффекты, возникающие вследствие высвобождения воспалительных медиаторов и цитокинов.
- Процессы взаимодействия лейкоцитов и эндотелиальных клеток, вследствие чего высвобождается большое количество переформированных и снова синтезируемых адгезивных молекул.
- Появление антител к фосфолипидам. Такие антитела обнаруживают у больных системным васкулитом. Отмечается их перекрестная реакция с эндотелиальными белками, что приводит к увеличению коагулирующих свойств крови.
Высокие кардио-риски при коронавирусе
Согласно исследованию, опубликованному в журнале JAMA Cardiology, в котором анализировали МРТ сердца 100 человек, вылечившихся от COVID-19, аномалии сердца обнаружены у 78% выздоровевших пациентов, а «продолжающееся воспаление миокарда» — у 60%. В том же исследовании у 76% обследованных пациентов был обнаружен высокий уровень фермента тропонина в крови, индикатора повреждения сердца. Большинству пациентов в исследовании не требовалась госпитализация.
Американские кардиологи — Грегг Фонаров, руководитель отделения кардиологии Калифорнийского университета в Лос-Анджелесе, и Мина Чанг, кардиолог и профессор медицины клиники Кливленда, Медицинский колледж Лернера — советуют выздоравливающим от COVID-19 следить за следующими симптомами:
- сильная одышка, невозможность лежать ровно без одышки и пробуждение ночью с одышкой;
- отек лодыжек;
- приступы головокружения.
Галина Семенова, кандидат медицинских наук, заведующая 11-м неврологическим отделением Покровской больницы, Санкт-Петербург:
Пациентов с инсультами стало больше, а сами инсульты стали протекать более тяжело. Обусловлено это в первую очередь тем, что коронавирус увеличивает свертываемость крови и способствует тромбообразованию. Как следствие, у пациентов усугубляются все сосудистые проблемы. Стало больше и инсультов, и инфарктов, больше тромбозов сосудов, независимо от того, где эти сосуды находятся (в головном мозге, миокарде, печени, почках, кишечнике, селезенке).
Лечение пациентов с коронавирусом проводится в соответствии с 9-й версией Временных методических рекомендаций МЗ РФ. Там указано, что профилактические дозы низкомолекулярных гепаринов (препараты, разжижающие кровь) должны назначаться всем госпитализированным пациентам.
1.Что такое васкулит и его возможные причины
Васкулит – это общий термин, описывающий группу заболеваний, характерной чертой которых является воспаление стенок кровеносных сосудов с последующим их разрушением. В основе этого болезненного состояния лежит нарушение работы иммунной системы, которая без каких-либо причин начинает видеть «опасность» в собственных кровеносных сосудах. Возникающие на фоне подобных сбоев воспалительные процессы способствуют ослабеванию сосудов, ухудшению эластичности их стенок, из-за чего они могут, как растянуться, так и сузиться вплоть до полного смыкания.
Васкулит может возникать у людей разных возрастных групп. Как правило, его появление обусловлено рядом аутоиммунных заболеваний соединительной ткани. Согласно статистическим исследованиям, у 5% больных васкулит появился из-за основного заболевания – хронического артрита. Еще чаще васкулит возникает на фоне синдрома Фелти – осложнения ревматоидного артрита.
С чем связано появление васкулита?
К сожалению, нельзя назвать точную причину васкулита. Однако в некоторых случаях удается установить взаимосвязь этого заболевания с ранее перенесенной или до сих пор присутствующей в организме человека вирусной инфекцией. В медицинской практике были зафиксированы случаи, когда васкулит являлся следствием серьезных аллергических реакций на медикаментозное лечение. Перечислим и другие факторы, провоцирующие образование васкулита:
- инфекционные заболевания;
- аллергические проявления на различные раздражители;
- генетическая предрасположенность;
- заболевания соединительной ткани;
- ожоги и травмы;
- ионизирующая радиация;
- повышенная вязкость крови и многое другое.
Артериит Такаясу
Известен также как неспецифический аортоартериит, или болезнь отсутствия пульса, — это облитерирующий васкулит, поражающий аорту и сосуды, отходящие от нее.
В стенках сосудов откладываются иммунные комплексы. Развиваются воспалительные гранулемы в адвентиции и наружных слоях средней оболочки сосудов, включающие скопления лимфоцитов, моноцитов и, частично, нейтрофилов, гигантских клеток и др. Гранулемы фиброзируются. Происходит тромбообразование, склерозирование средней оболочки, пролиферация интимы и, как следствие, сужение просвета сосудов.
Симптомы
Страдают в основном молодые женщины. В патологический процесс вовлекаются грудная аорта и ее ветви. Часто поражаются сосуды шеи и верхних конечностей. Формируются аневризма, тромбоз. Стеноз сосудов обусловливает хромоту, уменьшение или отсутствие пульса, гипертонию (частое поражение почечной артерии), несоответствие артериального давления между правой и левой руками. Возможно развитие лихорадки, миалгии, артралгии, головной боли и офтальмологических расстройств.
Лабораторная диагностика не имеет решающего значения. Отмечается увеличение СОЭ.
Лечение. Назначают кортикостероиды (преднизолон).