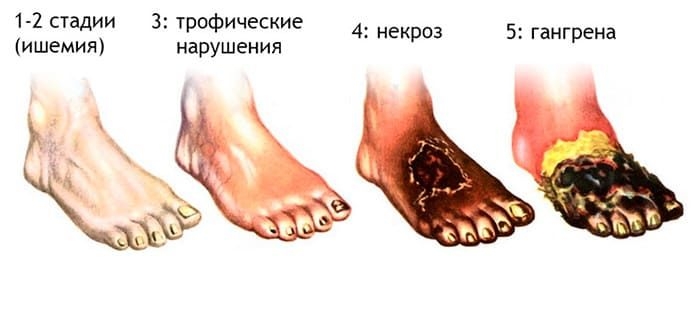
Дефект межжелудочковой перегородки (дмжп, врожденный порок сердца, роже болезнь, эйзенменгера синдром)
Содержание:
Аномалии положения сердца плода
Среди аномалий расположения сердца выделяют эктопию сердца (размещение вне грудной клетки). К таким патологиям относят декстрокардию (смещение сердца в правую сторону относительно нормального положения) и мезокардию (расположение сердца не с левой стороны грудины, а по срединной линии тела).
Эктопия сердца у плода возникает на сроке 14-18 дней с момента зачатия мезадерма начинает развиваться неправильно, что вызывает неправильное срастание брюшной стенки. У плода либо отсутствует диафрагма вообще, либо нет диафрагмального сегмента перикарда.
Из-за отверстия в стенке между правым и левым желудочком слышны интракардиальные шумы. Также у плода эктопия сердца нередко сопровождается другими аномалиями — гидроцефалией, энцефалоцеле и пр.
Надо сказать, что существует высокая вероятность ошибочного диагноза по установки положения сердца. При тазовом предлежании плода на УЗИ сердца визуализируется справа, хотя на самом деле оно располагается в положенном месте.
В 71% случаев эктопия сердца вызывается плевральным выпотом, кистозным аденоматозным пороком развития лёгкого, диафрагмальной грыжей.
Различают четыре вида эктопии:
- абдоминальная (сердце находится в брюшине);
- грудная (сердце выходит наружу через дефекты грудины);
- торакоабдоминальная (пентада Кантрелла – сложнейшая патология, имеющая комплекс отклонений от нормы);
- шейная (сердце смещается в область сердца).
Грудная эктопия встречается в 55-60% случаев, торакоабдоминальная — в 38%, шейная — почти в 3%. Выживаемость составляет около 10%. В большинстве случаев при эктопии младенец либо рождается мёртвым, либо умирает сразу после рождения.
Патология сопровождается смещением других внутренних органов, которые не защищены от механических повреждений и подвержены инфекциям и вирусам больше обычного.
Часто задаваемые вопросы
Каким способом производится обезболивание при операции?
Анестезия может быть как местной, так и общей. Выбор зависит от решения врачей, которые будут проводить эту операцию. Если пациент хорошо переносит общий наркоз, то вполне возможен этот вариант, чтобы исключить волнение и неприятные ощущения.
Как осуществляется контроль за выполнением эндоваскулярного вмешательства?
Достаточно часто требуется уточнение строения дефекта, тогда на этом этапе выполняют ангиографию – рентгеноконтрастное исследование сосудов. Окклюдер подбирают индивидуально, его помещают в катетер и доводят до сердца. Затем, под контролем с помощью видеоизображений, производится установка и раскрытие окклюдера.
Если требуется дополнительный контроль над работой сердца, то используют эхокардиограф с датчиком, помещаемым в пищевод. Чреспищеводная Эхокардиография позволяет наблюдать за состоянием сердечной мышцы в режиме реального времени.
Как проводится реабилитация после манипуляции?
Общий срок проведения операции – не более 1,5-2 часов. Обычно процедура занимает около часа. Госпитализация производится на срок от суток до недели – зависит от индивидуального состояния пациента. После операции назначают прием антикоагулянтов – препаратов, препятствующих образованию тромба, а также антибиотиков, которые позволяют избежать бактериальной инфекции сердца.
Если в послеоперационном периоде не возникает осложнений, то требуется контрольное обследование через 3-4 недели. Иногда возникают такие симптомы, как боли и одышка. При появлении осложнений необходимо обратиться к лечащему врачу – при правильно проведенной операции побочные эффекты не развиваются.
Причины
- Инфекционные болезни матери в первые три месяца беременности: корь, краснуха, ветрянка.
- Употребление алкоголя и наркотических препаратов.
- Некоторые лекарственные средства: варфарин, препараты содержащие литий.
- Наследственная предрасположенность: порок сердца передается по наследству в 3-5% случаев.
- Множественные мелкие отверстия – самая легкая форма, которая мало влияет на состояние здоровья.
- Множественные крупные отверстия. Перегородка напоминает швейцарский сыр – самая тяжелая форма.
- Отверстия в нижней части перегородки, состоящей из мышц. Они чаще других затягиваются самостоятельно в течение первого года жизни ребенка. Этому способствует развитие мышечной стенки сердца.
- Отверстия, находящиеся под аортой.
- Дефекты в средней части перегородки.
Правый желудочек
Функциональная анатомия правого желудочка
Объем правого желудочка у новорожденных составляет 8,5-11 см3,
у детей первого года жизни — 13-20 см3, в 7-9 лет — 28-40 см3,
к 18 годам достигает 150-225 см3. У новорожденных и детей до
1 года длина правого желудочка составляет 4,3-6,2 см, ширина 2,1-3,2
см, у 7-12 летних детей длина желудочка увеличивается до 5-7,2 см,
ширина — до 2-3,5 см. К 18 годам длина правого желудочка достигает
7,3-9,2 см, ширина — 3-5 см. Толщина свободной стенки правого желудочка
у детей до 1 года равна 0,1-0,16 см, к 6 годам она возрастает до 0,2
см, а к 12 годам достигает 0,32 см. Полость правого желудочка имеет
выраженную трабекулярность, при этом основания сосочковых мышц располагаются
в толще трабекул.
Одномерная эхокардиография правого желудочка
Приточный отдел правого желудочка изучают в I стандартной позиции,
отточный в IV позиции. Поперечный размер правого желудочка по данным
эхометрии не соответствует анатомическому поскольку ультразвуковой
луч пересекает полость желудочка в зоне соответствующей 1/3 максимального
поперечного диаметра сферы. Толщина свободной стенки правого желудочка
в одномерном и двухмерном изображении обычно больше, чем анатомическая
из-за выраженной трабекулярности полости. Нормальные значения полости
правого желудочка и толщины его свободной стенки представлены в таблицах
5, 8, 15.
Семиотика правого желудочка
Дилатация правого желудочка
- Идиопатическая дилатация легочной артерии.
- Врожденное отсутствие клапана легочной артерии.
- Частичное отсутствие перикарда.
- Дефект межпредсердной перегородки (первичный, вторичный).
- Аномальный дренаж легочных вен (частичный, тотальный).
- Аномалия Эбштейна (имеется в виду увеличение атриализированной
порции желудочка). - Недостаточность трикуспидального клапана.
- Недостаточность клапана легочной артерии.
- Фистула правой коронарной артерии в правый желудочек.
- Врожденное отсутствие клапана легочной артерии.
- Опухоль правого желудочка.
- Синдром гипоплазии левого желудочка.
- Транспозиция магистральных сосудов.
- Легочная гипертензия (первичная, вторичная).
- Миокардит.
- Застойная сердечная недостаточность.
- Рестриктивная кардиомиопатия.
- Изменение позиции сердца (ротация правого желудочка
кпереди).
Уменьшение полости правого желудочка
- Атрезия трикуспидального клапана.
- Тампонада перикарда.
- Атрезия легочной артерии с интактной межжелудочковой
перегородкой. - Концентрическая гипертрофия правого желудочка.
- Аневризма межжелудочковой перегородки.
- Сдавление правого желудочка объемным образованием
средостения. - Изменение позиции сердца (ротация правого желудочка
кзади).
Гипертрофия свободной стенки правого желудочка
(увеличение толщины стенки более 3 — 5 мм)
- Стеноз легочной артерии (инфундибулярный, клапанный,
надклапанный, стеноз левой или правой ветви легочной артерии). - Легочная гипертензия (первичная, вторичная).
- Рестриктивная кардиомиопатия.
- Опухоль правого желудочка.
- Тетрада Фалло.
- Транспозиция магистральных сосудов.
- У новорожденных, рожденных от матерей,страдающих
диабетом. - Гипертрофическая кардиомиопатия с обструкцией выходного
тракта правого желудочка.
Дополнительные эхосигналы в полости правого желудочка
- Аномальные мышечные пучки.
- Опухоли правого желудочка (чаще рабдомиомы).
- Разрыв аневризмы синуса Вальсальвы в полость правого
желудочка. - Аневризма межжелудочковой перегородки.
- Тромб в правом желудочке.
Двухмерная эхокардиография правого желудочка
Правый желудочек визуализируют во взаимно перпендикулярных осях сканирования:
приточную порцию — в проекции 4-х камер с верхушки и поперечном парастернальном
сечении; отточную — в парастернальной проекции выходного тракта
правого желудочка и поперечном сечении на уровне магистральных сосудов.
Объемная перегрузка правого желудочка
- Дилатация правого желудочка.
- Парадоксальное движение межжелудочковой перегородки
(см) (при наличии легочной гипертензии может не определяться). - Увеличение экскурсии передней створки трикуспидального
клапана. - Систолическое трепетание трикуспидального клапана.
- Уменьшение амплитуды и скорости открытия передней
створки митрального клапана.
Гипертрофия правого желудочка
- Увеличение толщины свободной стенки правого желудочка
более 5 мм. - Гипертрофия (правосторонняя) межжелудочковой перегородки.
- Повышенная трабекулярность полости правого желудочка.
Прогноз и возможные осложнения
Если вовремя не провести лечение ДМЖ, возникают различные последствия:
- легочная гипертензия;
- синдром Эйзенменгера – необратимая легочная гипертензия вследствие сброса крови слева направо;
- сердечная недостаточность, в том числе острая;
- эндокардит – воспаление внутренней оболочки сердца;
- тромбоз;
- инсульт;
- развитие дополнительных клапанных пороков сердца;
- летальный исход.
Если дефект не был обнаружен во младенчестве, то о себе он даст знать ближе к 20-ти годам пациента, а осложнения будут достаточно серьезными и часто необратимыми. Всевозможные последствия и осложнения ДМПП приведены в таблице ниже.
| Возможные осложнения | Характеристика заболевания |
| Легочная гипертензия | Перегружается правая часть сердца, легочный круг застаивается, а давление в нем резко повышается. |
| Сердечная недостаточность | Сердце перестает качественно качать кровь. Насос не работает, клетки организма недополучают кислородного питания. |
| Аритмия | Сердечный ритм увеличивается, затем резкий перепад и снова увеличение темпа. Изменения чреваты летальным исходом из-за внезапной остановки сердца. |
| Синдром Эйзенменгера | Последствие легочной гипертензии. |
| Тромбоэмболия | Возникновение тромбов на любом из участков сосудов. Возможно закупорка жизненно важных артерий и мгновенная смерть. |
Чем раньше будет обнаружена патология, тем меньше вероятность развития тяжелых последствий ДМПП Отверстия, размер которых не превышает 6 или 7 мм, обычно зарастают. Большие дефекты у ребенка способны спровоцировать развитие:
- кровоизлияния в мозг;
- эндокардита;
- легочной гипертензии;
- дисфункции клапана;
- тромбоза.
После окончания лечения, выполнения рекомендаций врача прогноз благоприятный, у ребенка появляются все шансы на нормальную жизнь. При отказе от хирургического лечения большого дефекта в перегородке человек умирает до 25–27 лет.
Факторы развития
Заболевание встречается, как самостоятельная патология, так и совмещенная с иными дефектами развития органа. Нарушения появляются уже в эмбриональном периоде, когда происходит формирование системы кровообращения в первом триместре беременности матери. Повлиять на естественный механизм нормального развития способны любые неблагоприятные факторы внешней и внутренней природы:
- генетическая предрасположенность, семейственность сердечных пороков, наличие старших родственников с синдромом Холта-Орама;
- вирусные болезни матери;
- эндокринные нарушения в организме женщины (особенно диабетический синдром);
- систематическое отравление плода запрещенными медикаментами, алкоголем;
- проживание и работа в экологически неблагоприятных местностях;
- повышенный радиационный фон в местах постоянного пребывания;
- осложнения беременности (угрозы прерывания, патологические токсикозы).
В перегородке между предсердиями может быть одно или несколько отверстий разного диаметра. От размеров просвета зависит скорость развития сердечно-легочных нарушений в работе органов, развитие дыхательной недостаточности и цианоза (посинения кожных покровов даже в состоянии покоя). Из-за неправильного распределения давления в предсердиях происходит выбухание правой стороны сердца, что приводит к сужению легочной артерии, повышению давления, дыхательной недостаточности.
Причины дефекта межпредсердной перегородки
В основе формирования дефекта межпредсердной перегородки лежит нарушение развития первичной или вторичной перегородки в эмбриональном периоде.
- Первичный дефект располагается в нижней части межпредсердной перегородки рядом с фиброзными кольцами атриовентрикулярных клапанов (митрального и трехстворчатого), по сути его нижним краем является само фиброзное кольцо.
- Вторичный дефект располагается в центральной части межпредсердной перегородки, и все его края представлены самой перегородкой.
- Дефект венозного синуса – это дефект, локализующийся в верхней части межпредсердной перегородки. Данному пороку часто сопутствует аномальный дренаж лёгочных вен (часть лёгочных вен впадает не в левое предсердие, а в верхнюю полую вену).
Совет врача
Неоднократно родители терзали себя и меня, пытаясь выяснить точную этиологию врожденного порока у ребенка. Когда такой диагноз обнаруживают у родного малыша, хочется непременно найти виновного. Бабушка с папиной стороны иногда обвиняет невестку в «плохой генетике», мамина родня — зятя в курении и употреблении алкоголя.
Категорически не советую вам этого делать
Конечно же, причину узнать важно для того, чтобы прогнозировать рождение здоровых или больных детей у родителей и самого ребенка. Малыш с ДМЖП когда-нибудь сам станет отцом или матерью
Но болезнь маленького человека – не повод для выяснения отношений. Забудьте семейные ссоры. Сосредоточьтесь на заботе о малютке.
9.1. ДЕФЕКТ МЕЖЖЕЛУДОЧКОВОЙ ПЕРЕГОРОДКИ
ДМЖП — наличие сообщения между левым и правым желудочками, приводящее к патологическому сбросу крови из одной камеры сердца в другую. Дефекты могут располагаться в мембранозной (верхней) части межжелудочковой перегородки (75-80% всех дефектов), в мышечной части (10%), в выносящем тракте правого желудочка (надгребневые — 5%), в приносящем тракте (дефекты предсердно-желудочковой перегородки — 15%). Для дефектов, расположенных в мышечной части межжелудочковой перегородки, используют термин «болезнь Толочинова-Роже».
Распространённость
ДМЖП — наиболее частый врождённый порок сердца у детей и подростков; у взрослых он встречается менее часто. Это связано с тем, что в детском возрасте пациенты подвергаются оперативному вмешательству, у части детей ДМЖП закрываются самостоятельно (возможность самостоятельного закрытия сохраняется даже в зрелом возрасте при малых дефектах), а значительная часть детей с большими дефектами погибает. У взрослых обычно выявляют дефекты малого и среднего размера. ДМЖП может сочетаться с другими врождёнными пороками сердца (в порядке убывания частоты): коарктация аорты, ДМПП, открытый артериальный проток, подклапанный стеноз лёгочной артерии, подклапанный стеноз устья аорты, стеноз митрального отверстия.
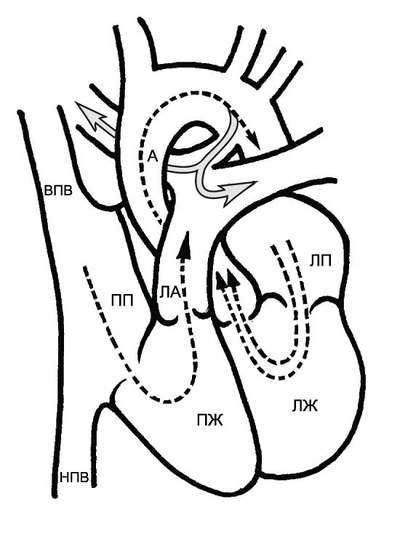
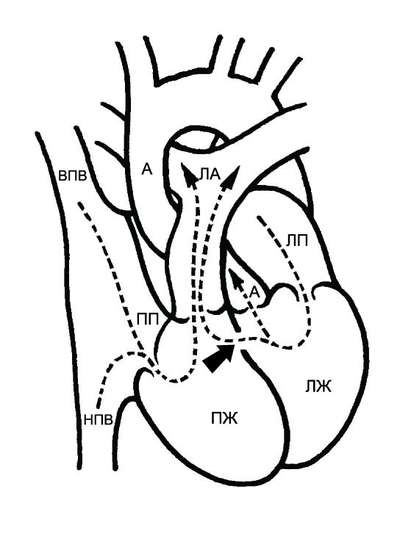
ГЕМОДИНАМИКА
У взрослых ДМЖП сохраняются в связи с тем, что они либо не были выявлены в детском возрасте, либо не были своевременно прооперированы (рис. 9-1). Патологические изменения при ДМЖП зависят от размеров отверстия и сопротивления лёгочных сосудов.
Лечение дефекта межпредсердной перегородки
На данный момент существует два вида оперативного лечения: 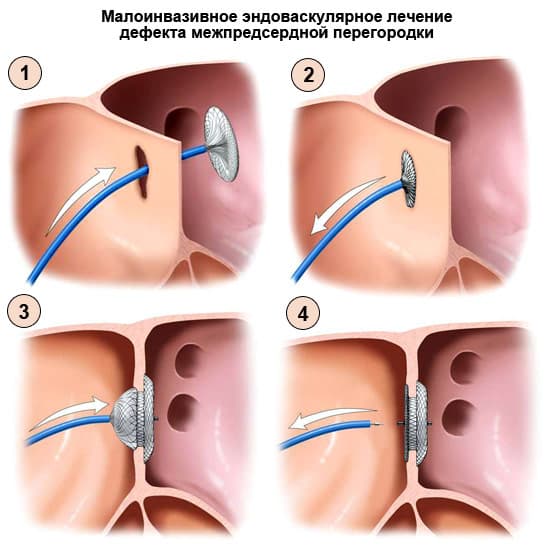
- 1. Операция на открытом сердце в условиях искусственного кровообращения с ушиванием дефекта или его пластикой заплатой из перикарда.
- 2. Устранение дефекта межпредсердной перегородки с использованием специальных устройств (окклюдеров) в условиях рентгеноперационной через проколы артерий без стернотомии.
- Необходимо понимать, что не каждый дефект может быть устранен оперативным путем, существуют противопоказания к операции (дефекты малого диаметра, тяжелая легочная гипертензия, право-левый сброс через дефект), и не каждый дефект может быть устранен с использованием оккклюдеров (сочетание дефекта с аномальным дренажом легочных вен, первичные дефекты с отсутствующим нижним краем, дефекты большого размера, сочетание дефекта с другой
- патологией сердца являются показанием к открытой операции).
- Более подробно о конкретном случае заболевания, показаниях и противопоказаниях можно узнать в процессе консультации сердечно-сосудистого хирурга (на амбулаторном приеме).
Симптомы дефекта межжелудочковой перегородки у новорожденных
Клиническая картина ДМЖП у новорожденных определяется диаметром сообщающего отверстия. Если он не превышает 10 мм, дети развиваются по возрасту. У них может слегка проявляться повышенная утомляемость, одышка. Со временем наблюдается выпячивающий «сердечный горб» — бугорок в грудной клетке.
Если дефект межжелудочковой перегородки у новорожденных имеет большие размеры, клиника развивается в первые месяцы жизни. Болезнь сопровождается такими признаками:

- синюшность периоральной зоны;
- потливость;
- одышка даже в покое;
- повышенная усталость;
- слабость;
- замедление физического развития, слабый рост;
- тахикардия;
- бледность кожи.
При грудном кормлении такие дети отрываются от бутылочки или груди, захватывают воздух.
Дефект межжелудочковой перегородки у новорожденных приводит к повторяющимся ОРЗ, инфекционным патологиям. В 3-4 годам детей начинают беспокоить боли в сердце, прослушиваются шумы. Границы сердца увеличиваются.
Врождённые дефекты сердца
Пять наиболее встречаемых дефектов — это тетрада Фалло, дефект межжелудочковой перегородки, транспозиция магистральных сосудов, коарктация аорты, гипоплазия левых камер.
Оптимальным сроком для проведения ультразвуковой диагностики сердца плода считается период 24-26 недель беременности. Именно в это время анатомические структуры сердца максимально визуализируются, а на более ранних сроках можно увидеть только явные и глобальные пороки сердца.
Наиболее информативен ультразвуковой осмотр 4-камерного среза сердца. После которого при любом отклонении от нормы женщина отправляется на более детальное обследование плода с использованием допплеровской эхокардиографии. Также проводится кариотипирование, потому что в 30% случаев аномалии являются результатом хромосомных нарушений.
Случай из практики
В родильном отделении неонатолог заподозрила врожденную патологию сердца. Ультразвуковое обследование выявило мышечный дефект межжелудочковой перегородки у новорожденной. Специалисты кардиоцентра рекомендовали провести оперативную коррекцию до 6-месячного возраста, так как размер отверстия оказался слишком велик. Родители настроились на хирургическое лечение, но, согласно их вере, требовалось благословение пастора. А тот, увидев вполне с виду здоровую девочку, посоветовал немного повременить с операцией. Мол, она ещё совсем маленькая, порок её не беспокоит, «разрезать» всегда успеете.
На седьмом месяце жизни у малышки появились первые признаки легочной гипертензии, с которой мы пытались безуспешно бороться назначением медикаментов. На девятом — родители умоляли кардиохирургов спасти ребенка, но оперировать было поздно — развилась клиника сердечной недостаточности. В годик девочка умерла.
А вчера на прием пришел юноша. Восемнадцать лет. Возмущался, что врачи призывной комиссии его отправили на дополнительное обследование в больницу. Занимается легкой атлетикой. Мечтает поступить в военное училище. Открываю амбулаторную карту, а там – оперативное лечение по поводу ДМЖП. На груди – тонюсенькая полоска послеоперационного шрама, практически незаметная. Парень операции не помнит. Искренне не понимает, чем он болен. Просто родители в свое время не побоялись его «разрезать».
Методы диагностики
Аускультативные данные и другие симптомы позволят педиатру заподозрить врожденный порок развития у ребенка. Скорее всего, детский кардиолог для уточнения диагноза выпишет направление на:
- Рентгенографию органов грудной клетки – при малом дефекте изменений не обнаружится. Если отверстие значительных размеров, могут выявиться гипертрофия левого предсердия и желудочка, усиление рисунка легких. В случае осложнения ДМЖП легочной гипертензией -выбухание дуги легочной артерии при ослаблении рисунка легких и негипертрофированном левом желудочке.
- Электрокардиографию – в дифференциации порока сердца не имеет особого значения, но позволит выявить отклонение электрической оси, а также признаки перегрузки обоих либо лишь левого желудочка.
- Эхокардиографию – считается главным диагностической технологией при сердечных пороках. Ультразвуковой метод обследования позволяет уточнить точную локализацию отверстия, его размеры, количество дефектов, а также оценить изменения гемодинамики. Основная задача проведения УЗИ – непосредственная визуализация порока, исключение других аномалий сердца. Допплеровское картирование поможет установить величину сброса, наличие регургитации крови, оценить систолическое давление в правом желудочке.
Если на ЭхоКГ дефекты видны недостаточно хорошо, или врач заподозрил комбинированный порок сердца, возможно, понадобится пройти магнитно-резонансную либо компьютерную томографию.
Катетеризация сердца и ангиография
Обычно детям эти диагностические методики назначаются редко, но, если неинвазивные методы не дают полной информации о состоянии, выполняются для оценки гемодинамики в малом круге кровообращения и легочной гипертензии. При данной процедуре измеряется давление в аорте, легочной артерии, определяется газовый состав крови внутри сердечных камер и крупных сосудов. Проводится опытными специалистами в регионарных центрах.