Печень
Содержание:
Симптоматика
Опухоль ворот печени по стадиям классифицируется отдельно от остальных анатомических структур билиарного тракта:
- Стадия 0 или in situ представляет собой выраженную дисплазию внутрипротоковой слизистой, как правило. это диагностическая находка при удалении желчного пузыря;
- 1 стадия — раковые клетки не выходят за пределы стенки протока, то есть, это четко отграниченное и сугубо внутрипротоковое поражение;
- 2 стадия — распространение злокачественного процесса за пределы желчного протока, но без вовлечения близлежащих анатомических структур, то есть раковые клетки могут быть только в окружающей жировой клетчатке;
- 3 стадия — распространение рака на сосуды или метастазы не более чем в трёх лимфатических узлах ворот при любом размере первичной опухоли;
- 4 стадия — при любом размере новообразования имеются метастазы в 4 лимфоузлах или отдалённые, в том числе печеночные, метастазы.
В подавляющем большинстве случаев главное проявление холангиокарциномы желчного протока — нарушение его проходимости с развитием механической желтухи. Симптомы желтухи фактически становятся проявлением опухоли Клацкина: изменение цвета кожи и белков глаз, кожный зуд, светлый кал при темной моче и, конечно, нарастающие симптомы интоксикации с повышением температуры тела.
До появления желтушности пациента может беспокоить прогрессивно нарастающая слабость и снижение аппетита при ощущении тяжести в правом подреберье. Характерна плохая переносимость жирных, жареных и мучных блюд, в том числе подташнивание, отрыжка горьким. Возможны эпизоды спастических болей в правом подреберье в сочетании с тошнотой и рвотой, нарушение стула — чаще диарея.
До развития желтухи биохимический анализ крови может выявить повышение уровня билирубина и трансаминаз, в моче появляются желчные кислоты. Опухолевые маркеры не характерны для холангиокарцином, но возможно небольшое повышение уровня СА 19-9, отражающее любую патологию билиарного тракта.
Препараты от боли в печени – что выбрать?
Чтобы вылечить боль в печени, нужно найти причину и вылечить основное заболевание. Диагностикой и лечением печени занимается врач-гастроэнтеролог. Врач проведет УЗИ печени и назначит несколько анализов, показывающих наличие воспаления, паразитов и печеночных компонентов, концентрация которых повышается при определенных патологиях. Также нужно будет провериться на гепатит.
Получив все результаты, можно будет понять, почему болит печень и чем ее лечить. Иногда достаточно пропить лекарства, улучшающие отток желчи. В других случаях требуются антибиотики, средства против лямблий. При тяжелых случаях проводят переливание крови и даже пересадку печени.
При своевременном обращении и выявлении патологии можно будет обойтись медикаментозным лечением с применением желчегонных средств, ферментов и растительных препаратов.
Препараты и травы, для лечения печени доступные без рецепта, содержат несколько компонентов:
- расторопшу – облегчает выработку желчи;
- экстракт артишока – оказывает слегка детоксицирующее действие на организм, улучшает переваривание пищи;
- экстракт корня цикория – очищает организм, выводит из организма свободные радикалы и снижает уровень холестерина;
- холин – компонент фосфолипидов, являющихся строительными блоками клеточных мембран гепатоцитов;
- экстракт зеленого чая – влияет на регенерацию печени, подавляет фиброз клеток печени.
ОНЛАЙН-ЗАПИСЬ в клинику ДИАНА
Вы можете записаться по бесплатному номеру телефона 8-800-707-15-60 или заполнить контактную форму. В этом случае мы свяжемся с вами сами.
Анатомия и строение
Анатомия — наука, которая изучает внешнее и внутреннее строение печени. Охарактеризуем кратко основные положения. Она имеет две доли, между которыми находится серповидная связка печени и продольные борозды. Правая доля весит больше левой. На задней поверхности находится венечная связка. Две борозды делят ее на вторичные доли. Диафрагмальная поверхность имеет сердечное вдавление и 4 части. Висцеральная — разделена тремя бороздами на четыре доли. На ней находится продольная борозда с ямкой для желчного пузыря и вдавления для соседних органов. У ворот печени находится поперечная борозда, откуда выходят общий печеночный проток и лимфатические сосуды печени, а заходят — нервы, собственная печеночная артерия и воротная вена, круглая связка печени, которая находится в борозде. Снаружи она покрыта серозной оболочкой, под ней — фиброзной капсулой.
Внутренняя анатомия начинается с того, что соединительная капсула заходит в ворота печени и делит ее на доли, сегменты и дольки. Гистология печени описывает ее клеточное строение. Печеночная долька — основная структурная единица, имеющая форму призмы. Вена и желчные протоки, которые содержит клетка, а также междольковые артерии образуют триаду. По периферии от нее располагаются печеночные балки продолговатой формы. Клетки печени имеют ядро и набор хромосом. В печени человека содержится 250—300 млрд гепатоцитов. Дольки разделены междольковой перегородкой из соединительной ткани, в которой проходят желчный капилляр и сосуды. Объединяясь между собой, образуют 8 сегментов и 5 секторов.
Стадии, классификация
Стадию опухоли Клацкина определяют в соответствии с общепринятой системой TNM, которая предусматривает оценку размера и других характеристик первичной опухоли (T), поражения регионарных лимфатических узлов (N), наличия отдаленных метастазов (M).
Выделяют следующие стадии заболевания:
- Стадия 0: рак «на месте», злокачественная опухоль, которая не распространяется за пределы слоя клеток, выстилающих изнутри желчные протоки.
- Стадия I: злокачественная опухоль, которая прорастает в мышечный, фиброзный слой желчных протоков, но не распространяется на соседние ткани.
- Стадия II: злокачественная опухоль, которая распространяется в окружающую жировую ткань или ткань печени.
- Стадия III: злокачественная опухоль распространяется на ветви печеночной артерии или воротной вены и/или присутствуют очаги в регионарных лимфатических узлах.
- Стадия IVA: злокачественная опухоль, которая вторгается в печеночную артерию, воротную вену, соседние желчные протоки и/или присутствуют очаги в регионарных лимфатических узлах.
- Стадия IVB: присутствуют очаги в лимфатических узлах чревной, брыжеечной артерии, периаортальных, перикавальных лимфоузлах, либо имеются отдаленные метастазы.
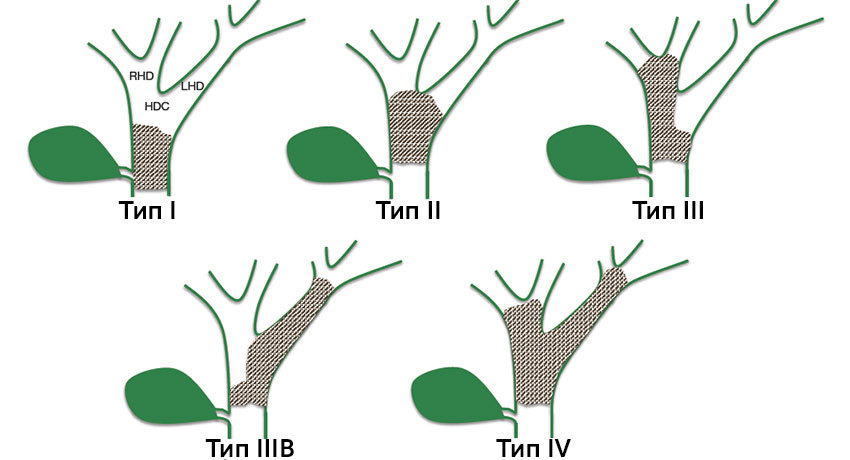
Кроме того, чтобы обозначить расположение злокачественной опухоли, при хилярных холангиокарциномах используют специальную классификацию по Висмуту — Корлетту:
- Тип I: злокачественное новообразование расположено дистальнее слияния правого и левого желчных протоков.
- Тип II: опухоль захватывает место слияния и частично правый и левый протоки.
- Тип III: злокачественная опухоль распространяется на общий печеночный проток и правый (IIIA) или левый (IIIB) проток.
- Тип IV: поражение общего, правого и левого печеночных протоков.
В зависимости от характера роста, опухоли Клацкина делят на три типа: склерозирующие, узелковые и папиллярные. Чаще всего встречаются склерозирующие — они растут в толщу стенки желчных протоков. Узелковые и папиллярные растут в просвет. Наиболее благоприятными считаются папиллярные, они чаще всего являются резектабельными.
Причины возникновения
У большинства пациентов развитию опухоли Клацкина предшествовали заболевания билиарного тракта — холангиты инфекционной, чаще всего паразитарной природы, или аутоиммунного характера. В отличии от злокачественного новообразования желчного пузыря, не найдено доказательств какой-либо связи с желчнокаменной болезнью.
Давно замечена высокая заболеваемость холангиокарциномой зараженных определенными гельминтами — печеночной двуусткой, паразитирующей в печени и поддерживающей хроническое воспаление протоков с исходом в склерозирование.
В качестве потенциального фактора риска опухоли общего желчного протока признаются воспалительные заболевания кишечника, чаще всего неспецифический язвенный колит, встречающийся у каждого двухсотого больного опухолью Клацкина.
Традиционно не исключается соучастие в злокачественной трансформации хронических гепатитов, как вирусных, так и алиментарных при злоупотреблении алкоголем, цирроза и жирового перерождения печени при ожирении. Курение сегодня признается одним из ведущих факторов риска любой злокачественной опухоли органов билиарного тракта.
Предполагается и наследственная предрасположенность, но из-за редкости заболевания достоверных доказательств этому пока не нашли.
Поскольку российская статистика учитывает все злокачественные новообразования билиарного тракта, без разделения на возникшие в протоке или желчном пузыре, по приблизительным подсчётам опухоль Клацкина ежегодно диагностируется у 1000-1200 россиян и не имеет гендерных предпочтений.
Разновидности новообразования
Опухоли желчных протоков, формирующих разветвленный билиарный тракт, анатомически разделяют на внутрипеченочные и внепеченочные, а карцинома Клацкина всегда внепеченочная. Большинство холангиокарцином возникает в желчном пузыре, и только треть в протоках. Половину всех протоковых раков составляют опухоли Клацкина.
Опухоль Клацкина по клеточной структуре в 90% случаев состоит из трансформировавшегося железистого эпителия, частота плоскоклеточного рака — менее 5%, ещё реже в этой области встречаются саркомы и лимфомы.
По типу роста в протоке различают следующие варианты:
- Чаще всего раковые клетки распространяются внутри стенки протока, циркулярно сужая просвет без образования четко очерченной опухоли. Такие новообразования называются склерозирующими, они типичны для протокового рака внепеченочной локализации.
- Гораздо реже раковая опухоль растёт в просвет протока в виде полипа, такую форму обозначают как папиллярная. Как правило, при таком типе течение опухоли Клацкина несколько благоприятнее, потому что рядом располагающиеся анатомические структуры вовлекаются в конгломерат чуть позже, сначала опухоль оттесняет их в сторону.
- Нодулярный вариант представляет собой смесь двух предшествующих, когда конгломерат опухоли сдавливает проток, но не типичен для злокачественного поражения внепеченочных протоков.
Опухоль Клацкина рано дает метастазы в лимфатические узлы ворот.
Развитие диагностики с внедрением КТ и МРТ позволило не только раньше выявлять патологии ворот печени, но и расширило спектр паллиативных вмешательств на билиарных протоках, что потребовало унификации анатомической классификации. Задачу отчасти выполняет система Бисмут-Колетт (Вismuth-Corlette), взявшая за основу расположение ракового образования относительно места слияния правого и левого печеночного протока в общий – бифуркацию.
По классификации Бисмут-Колетт:
- рак в общем протоке обозначается как I тип, по статистике самый частый – до половины всех случаев холангиокарциномы;
- опухоль бифуркации – II тип у каждого пятого больного;
- карцинома одного долевого – III тип, в зависимости от стороны поражения добавляется литера «А» или «В»;
- двустороннее вовлечение – IV, соотнести которое с традиционной классификацией TNM не представляется возможным.
Фокальная узловая гиперплазия (ФУГ)
Фокальная узловая гиперплазия (ФУГ) считается вторым (после гемангиом) наиболее распространенным доброкачественным новообразованием печени. По данным ряда авторов, ФУГ встречается у 0,9-5% населения, в 5-20% случаев может сочетаться с кистами и гемангиомами. Согласно литературным данным, ФУГ, не имея признаки опухоли, входит в группу доброкачественных гепатоцеллюлярных опухолей эпителиальной природы. Это одиночное, округлое, неинкапсулированное образование с нарушенной печеночной архитектоникой, разделенное септами, достигающими центрального рубца. Средние размеры очага – 5,7 см (от 1,5 до 12,0 см). Установлено, что ФУГ не склонна к кровоизлияниям и не имеет злокачественного потенциала. Обычно опухоль является случайной находкой при диагностических исследованиях. Узлы малых размеров, как правило, бессимптомны. Крупные опухоли могут вызывать боли в животе.
При нативном УЗИ в большинстве случаев ФУГ визуализируются с трудом, отображаясь в виде участка округлой формы с четкими контурами, изоэхогенной или незначительно гипо- или гиперэхогенной структуры. По мнению некоторых авторов, в диагностике ФУГ контрастное УЗИ является более информативной в отличие от других методов диагностики. Появление эхоконтрастных препаратов второго поколения значительно расширило возможности метода
Это позволяет дифференцировать различные типы опухолей, учитывая их характер васкуляризации, имеющего важное значение в дифференциальной диагностике очаговых образований печени. Повышенная васкуляризация опухоли в сочетании с характерным рисунком «колеса со спицами» является патогномоничным признаком ФУГ (71,4%)
При этом частота обнаружения «питающей» артерии опухоли увеличивается до 98%. Чувствительность и специфичность УЗИ с применением внутривенного контрастирования в диагностике ФУГ достигают 83 и 98% соответственно.
Гипоэхогенное образование в печени — доброкачественная фокальная нодулярная гиперплазия. В литературе описывают, что для нее характерен центральный рубец (белая стрелка).
В-режим. В IV сегменте печени, выходя на контур печени, деформируя его, визуализируется тканевой плотности гипоэхогенное, несколько неоднородное по эхоструктуре образование размерами 50 х 40 мм, неправильной формы, с четкими ровными контурами.
Методы лечения
Единственный метод лечения, который позволяет полностью избавиться от опухоли Клацкина и значительно повысить выживаемость — радикальная операция. К ней прибегают при I–II стадиях заболевания. Выполняют резекцию печени, удаляют желчные протоки и регионарные лимфатические узлы.
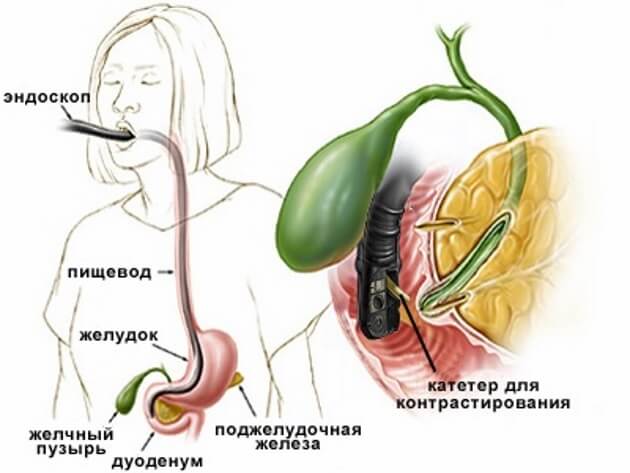
При механической желтухе операция сопряжена с высоким риском осложнений, поэтому предварительно нужно восстановить отток желчи. В настоящее время для этого зачастую прибегают к стентированию. В заблокированный участок желчных протоков устанавливают стент — небольшую трубку с сетчатой стенкой из металла. Для этого не нужно делать разрезов или проколов на брюшной стенке — манипуляцию проводят во время эндоскопии двенадцатиперстной кишки. Спустя 4–6 недель можно выполнить хирургическое вмешательство.
При резекции печени важно, чтобы осталась достаточно большая часть органа, которая могла бы справляться с его функциями. Если ожидается, что объем оставшейся печеночной ткани будет менее 25%, за 3–5 недель до хирургического вмешательства целесообразно провести эмболизацию ветвей воротной вены
За счет этого происходит гипертрофия ткани печени, и после операции удается сохранить ее больший объем. Это помогает предотвратить печеночную недостаточность.
Удаленную злокачественную опухоль отправляют в патоморфологическую лабораторию, где проводят гистологическое, иммуногистохимическое, молекулярно-генетическое исследование. Определяют мутации в генах BRAF, KRAS, ALK, транслокацию ROS1, Her-2new, микросателлитную нестабильность. Эти генетические изменения встречаются примерно в 10% случаев, и они делают злокачественную опухоль чувствительной к некоторым таргетным препаратам.
Некоторым пациентам с неоперабельной опухолью Клацкина может быть предложена трансплантация печени.
После операции может быть назначена адъювантная терапия, например, лучевая терапия в сочетании с химиопрепаратом 5-фторурацилом. В ряде исследований такой подход показал улучшение показателей выживаемости. В настоящее время нет доказательств того, что перед операцией была бы полезна неоадъювантная терапия — исследования на эту тему продолжаются.
При неоперабельном раке в области ворот печени применяют химиотерапию (обычно сочетание гемцитабина с препаратами платины), лучевую терапию.
В ряде случаев применяется фотодинамическая терапия (ФДТ). Пациенту внутривенно вводят особое соединение — фотосенсебилизирующий агент, который накапливается в раковых клетках, и затем активируют его с помощью света. В итоге образуются свободные радикалы, которые уничтожают опухолевые клетки.
Диагностические меры
Патологии ВВ выявляют с помощью УЗИ и МРТ
УЗИ-Доплера позволяет оценить характер движения крови, портальная вена просматривается у ворот печени, где она делится на 2 ветки. Кровь двигается в сторону печени. С помощью 3-D/4-D-УЗИ можно получить объёмное изображение сосуда. Нормальная ширина просвета ВВ во время ультразвукового исследования – около 13 мм. Проходимость сосуда имеет огромное значение в диагностике.
Также этот метод позволяет выявить гипоэхогенное (сниженная акустическая плотность) или гиперэхогенное (повышенная плотность) содержимое в портальной вене. Такие очаги свидетельствуют об опасных заболеваниях (ТВВ, цирроз, абсцесс, карцинома, рак печени).
При портальной гипертензии УЗИ покажет, что диаметр сосудов увеличен (это касается и размера печени), а в брюшной полости скопилась жидкость. С помощью цветного допплера можно выявить, что кровообращение замедлилось, появились кавернозные изменения (косвенный симптом портальной гипертензии).
Магнитно-резонансная томография полезна тем, что помогает определить причины изменений в системе воротной вены. Проводится осмотр паренхимы печени, лимфоузлов и окружающих образований. МРТ покажет, что в норме максимальный вертикальный размер правой доли печени составляет 15 см, левой – 5 см, билобарный размер у ворот печени – 21 см. При отклонениях эти значения меняются.
Один из самых эффективных методов диагностики ТВВ – это ангиография. При ПГ обязательно проводят фиброгастродуоденоскопию, эзофагоскопию, рентген с применением контрастного вещества для исследования пищевода или желудка.
Кроме инструментальных исследований, проводятся ещё и лабораторные. С их помощью обнаруживают отклонения от нормы (избыток лейкоцитов, повышение ферментов печени, сыворотка крови содержит большое количество билирубина и т. д.).
Строение печени
Снаружи печень покрыта серозной оболочкой, представленной висцеральной брюшиной. Небольшой участок в задней части не покрыт брюшиной — это внебрюшинное поле. Однако, несмотря на это, можно считать, что печень расположена интраперитонеально. Под брюшиной находится тонкая плотная фиброзная оболочка (глиссонова капсула) . Со стороны ворот печени фиброзная ткань проникает в вещество органа, сопровождая кровеносные сосуды. С учетом распределения кровеносных сосудов и желчных протоков в печени выделяют (по Куино, 1957) 2 доли, 5 секторов и 8 сегментов. В долях печени разветвляются соответствующие (правая и левая) ветви воротной вены. Согласно данным Куино, границей между правой и левой долями печени является условная плоскость, проходящая по линии, соединяющей ямку желчно- го пузыря впереди и борозду нижней полой вены сзади. Н левой доле выделяют З сектора и 4 сегмента, в правой — 2 сектора и также 4 сегмента. Каждый сектор представляет собой участок печени, в который входят ветвь воротной вены второго порядка и соответствующая ей ветвь печеночной артерии, а также нервы и выходит секторальный желчный проток. Под печеночным сегментом понимают участок печеночной паренхимы, окружающий ветвь воротной вены третьего порядка, соответствующие ей ветвь печеночной артерии и желчный проток. Левый дорсальный сектор, соответствующий первому (С 1) печеночному сегменту, включает хвостатую долю и виден только на висцеральной поверхности и задней части печени. Ллевый латеральный сектор (2-й сегмент — С II) охватывает задний участок левой доли печени. Левый парамедианный сектор занимает переднюю часть левой доли печени (3-й сегмент — С III) и ее квадратную долю (4-й сегмент — С IУ) с участком паренхимы на диафрагмальной поверхности органа в виде полосы, суживающейся кзади (к борозде нижней полой вены) . Правый парамедианный сектор представляет собой печеночную паренхиму, граничащую с левой долей печени. Н этот сектор входят 5-й сегмент (С У) , лежащий кпереди, и крупный 8-й сегмент (С УIII), занимающий заднемедиальную часть правой доли печени на ее диафрагмальной поверхности. Правый латеральный сектор, соответствующий самой латеральной части правой доли печени, включает 6-й- С УI (лежит впереди) и 7-й — С УII сегменты. Последний располагается позади предыдущего и занимает заднелатеральную часть диафрагмальной поверхности правой доли печени.
По своему строению печень — сложно разветвленная трубчатая железа, выводными протоками которой являются желчные протоки. Морфофункциональной единицей печени является долька печени. Она имеет форму призмы, размер ее в поперечнике от 1,0 до 2,5 мм. В печени человека таких долек около 500 000. Между дольками имеется небольшое количество соединительной ткани, в которой располагаются междольковые протоки (желчные) , артерии и вены. Обычно междольковые артерия, вена и проток прилежат друг к другу, образуя печеночную триаду. дольки построены ив соединяющихся друг с другом печеночных пластинок («балок») в виде сдвоенных радиально направленных рядов печеночных клеток. В центре каждой дольки находится центральная вена. Внутренние концы печеночных пластинок обращены к центральной вене, наружные — к периферии дольки. Между печеночными пластинками также радиально располагаются синусоидные капилляры, несущие кровь от периферии дольки к ее центру (к центральной вене). Внутри каждой печеночной пластинки между двумя рядами печеночных клеток имеется желчный проточек (каналец), являющийся начальным звеном желчевыводящих путей. В центре дольки (возле центральной вены) желчные проточки замкнуты, а на периферии долек они впадают в желчные междольковые проточки. Последние, сливаясь друг с другом, образуют более крупные желчные протоки. В конечном итоге в печени формируются правый печеночный проток, который выходит из правой доли печени, и левый печеночный проток, выходящий из левой доли печени. В воротах печени эти два протока сливаются, образуя общий печеночный проток, длиной 4-6 см. Между листками печеночно-двенадцатиперстной связки общий желчный проток сливается с пузырным протоком, в результате чего образуется общий желчный проток.
Что такое опухоль Клацкина
Опухоль Клацкина обобщённо — это рак ворот печени, а точнее — карцинома, развившаяся в желчных протоках, или холангиокарцинома.
Печеночные ворота — место вхождения внутрь органа более двух артерий с нервами, выхода наружу нескольких крупных вен, множества лимфатических сосудов и желчных протоков. Ворота небольшие по размеру — от 6 до 18 квадратных сантиметров.
Из каждой печеночной доли исходит по крупному желчному протоку, они сливаются в общий желчный проток. Опухоль Клацкина развивается либо в долевом протоке, либо в общем жёлчном протоке, протяжённость которого не превышает 5 см при несколько меньшем диаметре.
В воротах может развиться и опухоль печени, и протока или желчного пузыря, и метастазы в лимфоузлы. Все структуры взаимодействуют, поэтому при локальном новообразовании диагноз позволяет поставить только микроскопия опухоли.
Опухоль Клацкина не может развиться в ткани печени, она появляется только в слизистой оболочке протока, но быстро прорастает внутрь печени, сдавливая её сосуды и нервы, перекрывая просветы долевых желчных протоков.
Прогноз выживаемости
Опухоль Клацкина по-прежнему остается одним из «сложных» онкологических заболеваний с низкими показателями выживаемости. Средняя пятилетняя выживаемость после хирургического вмешательства составляет 10–40%. У многих пациентов уже во время операции становится понятно, что опухоль невозможно удалить полностью. И даже если по результатам биопсии получен негативный край резекции (рядом с линией разреза не обнаружено опухолевых клеток), впоследствии в 50–70% случаев происходит рецидив.
Тем не менее, совершенствуются хирургические вмешательства, появляются новые противоопухолевые препараты. Опухоли Клацкина встречаются редко, поэтому их сложно изучать, зачастую не удается собрать нужного количества пациентов, чтобы оценить статистику. Тем не менее, ученые продолжают искать новые подходы, новые эффективные методы лечения. В клинике Медицина 24/7 применяются все современные методики, новейшие препараты, у нас работают врачи, которые имеют большой опыт лечения холангиоцеллюлярного рака. В нашей клинике пациенты с этими заболеваниями могут получить наиболее эффективную помощь, в соответствии с современными международными стандартами.
Материал подготовлен врачом-онкологом, эндоскопистом, главным хирургом клиники «Медицина 24/7» Рябовым Константином Юрьевичем.