Антенатальное применение кортикостероидов с целью профилактики респираторного дистресс-синдрома новорожденных
Содержание:
Лечение
Специфическое лечение ОРДС отсутствует, и основная терапия направлена на лечение основного заболевания/стрессового фактора, вызвавшего ОРДС и на поддержание жизнедеятельности пациента. С этой целью проводится активная респираторная поддержка и фармакологическая терапия по показаниям.
Для купирования гипоксии проводится неинвазивная кислородотерапия через маску/носовой катетер. При недостаточной эффективности оксигенации/при тяжелых состояниях пациента, вызванных дыхательной недостаточностью/неспособностью пациента самостоятельно контролировать дыхание показана ИВЛ на фоне активной кинетотерапии (смена положения тела на живот/бок).
Назначение фармакологических препаратов определяется развивающейся клинической картиной и симптомами. Так, при сепсисе или инфекционных заболеваниях, вызвавших ОРДС показано назначение антибактериальных средств в зависимости от возбудителя и его чувствительности (Цефазолин, Ампициллин, Имипенем, Клиндамицин, Оксациллин и др.). Рекомендуется назначение респираторных фторхинолонов (Гатифлоксацин, Левофлоксацин).
На фоне респираторной поддержки, независимо от тяжести ОРДС, требуется инотропная поддержка гемодинамики. С этой целью назначаются Допамин, Дофамин. При отсутствии эффекта параллельно назначается титрование адреналина (норадреналина).
При появлении в системе гемостаза гиперкоагуляционных сдвигов необходимо назначать антикоагулянты (Гепарин, свежезамороженная плазма). Показано введение интратрахеально искусственного сурфактанта: Куросурф. Для стимуляции процессов образования/секреции сурфактанта пневмоцитами могут назначаться ингаляционные глюкокортикоиды (Беклометазон, Флутиказон, Будесонид, Мометазон), Бронхолитики (Аминофиллин), β2-адреномиметики пролонгированного действия (Салметерол, Онбрез, Формотерол). В фибропролиферативной стадии показан Метилпреднизолон в небольших дозах (2-3 мк/кг массы тела).
С целью седатации рекомендуется внутривенное введение таких препаратов как Мидазолам, Реланиум, Пропофол; при необходимости могут назначается мышечные релаксанты: Ардуан, Аперомид.
Доктора
специализация: Пульмонолог / Кардиолог / Рентгенолог / Неонатолог / Педиатр
Балыбердин Дмитрий Михайлович
2 отзываЗаписаться
Подобрать врача и записаться на прием
Лекарства
Куросурф
Мидазолам
Допамин
Дофамин
Цефазолин
Ампициллин
Ардуан
Аминофиллин
- Антибактериальные средства (Цефазолин, Ампициллин, Имипенем, Клиндамицин, Оксациллин, Гатифлоксацин, Левофлоксацин).
- Седативные средства (Мидазолам, Реланиум, Пропофол).
- Мышечные релаксанты (Ардуан, Аперомид).
- Препараты сурфактанта (Куросурф, Экзосурф, Порактант альфа, Бовактант, Берактант, Сурфактант БЛ).
β2-адреномиметики пролонгированного действия (Салметерол, Онбрез, Формотерол). - Ингаляционные глюкокортикоиды (Беклометазон, Флутиказон, Будесонид, Мометазон).
- Кардиотонические средства (Допамин, Дофамин).
- Бронхолитики (Аминофиллин).
Проведение оперативного вмешательства при ряде заболеваний, вызвавших ОРДС (травмы, хирургическая санация очага инфекции, переломы позвоночника/костей таза, черепно-мозговая травма и др.).
Лечение
Диагностика респираторного дистресс-синдрома проводится в условиях роддома.
Основой лечения детей с РДС является техника «минимальных прикосновений», ребенок должен получать только абсолютно необходимые ему процедуры и манипуляции. Один из методов лечения синдрома — интенсивная дыхательная терапия, различные виды искусственной вентиляции легких (ИВЛ) .
Логично было бы предположить, что раз РДС вызывается недостатом сурфактанта, то и лечить синдром нужно введением этого вещества извне. Однако это сопряжено с таким количеством ограничений и сложностей, что активное использование препаратов искусственного сурфактанта началось только в конце 80-х — начале 90-х годов прошлого века. Сурфактантотерапия позволяет намного быстрее улучшить состояние ребенка. Однако эти препараты очень дороги, эффективность их применения высока только если они используются в первые несколько часов после рождения и для их использования необходимо наличие современного оборудования и квалифицированного медицинского персонала, так как существует большой риск развития тяжелых осложнений.
Симптомы
Симптомы нейроциркуляторной дистонии очень разнообразны и лежат в основе классификации патологии. Тем не менее, можно выделить ряд общих признаков, которые характерны для большинства видов НЦД:
- частая смена настроения;
- постоянная усталость и сонливость;
- отсутствие сил, слабость;
- ощущение комка в горле;
- повышенное потоотделение;
- метеочувствительность;
- тревожность;
- ощущение нехватки воздуха и т.п.
Обострение заболевания может быть спровоцировано любой стрессовой ситуацией: избыток позитивных или негативных эмоций, недосыпом или даже простой сменой часовых поясов.
Симптомы синдрома вегетативной дистонии
Симптомы СВД напрямую зависят от того, какая система или какой орган были поражены. Заболевание приводит к дисфункции систем организма. По характеру течения у детей выделяют следующие отклонения:
Ваготония – нарушение нервной системы, которое проявляется акроцианозом стоп и кистей. Данная патология проявляется посинением конечностей. Причиной тому является чрезвычайно медленное поступление крови к конечностям через маленькие сосуды. Также симптомами СВД являются угревая сыпь, гипергидроз, а также аллергии и отеки под глазами. В случае депрессивного нарушения нервной системы кожа становится холодной, сухой и достаточно бледной, сосудистая сетка становится невыраженной. В некоторых случаях могут быть замечены экзематозное высыпание, зуд.
Характерным нарушением является отчетливое нарушение терморегуляции: плохая переносимость морозов, сырой погоды, сквозняков, а также постоянный озноб и зябкость.
Дети с синдромом вегетативной дистонии часто жалуются на плохую работу желудочно-кишечного тракта. Тошнота, боль в животе, рвота, изжога, понос или, наоборот, длительные запоры, боль за грудиной, ком в горле – привычное дело при СВД. Причиной этих нарушений является сокращение мышц пищевода и глотки. В зависимости от возраста ребенка самыми популярными симптомами синдрома вегетативной дистонии являются: боль в области живота – 6-12 лет; периодическая рвота – 3-8 лет; поносы и запоры – 1-3 года; колики и срыгивания – до 1 года.
Наиболее отчетливо СВД представлен нарушениями функции сердечно-сосудистой системы. Это состояние называется нейроциркуляторная дистония. При данном заболевании может быть огромное количество нарушений работы сердца, самые популярные из которых связаны с нарушением проводимости и сердечного ритма. Традиционно к дисфункции сердца относят:
Экстрасистолия – сокращение сердца раньше установленного времени. Среди всех аритмий детская экстрасистолия заметно лидирует: порядка 75% случаев приходятся именно на это нарушение. При экстрасистолии пациенты жалуются на головную боль, раздражительность, головокружение, чрезмерную утомляемость и так далее. Параллельно с этим возникают и другие заболевания и отклонения: высокая метеотропность, метеозависимость, а также вестибулопатия. Пациенты быстро утомляются при нагрузках, их работоспособность находится на очень низком уровне.
Пароксизмальная тахикардия – крайне внезапный симптом. Без адекватных на то причин сердце ребенка начинает стучать намного быстрее. Это может длиться как несколько часов, так и пару секунд. Чаще всего жертвами пароксизмальной тахикардии как следствия синдрома вегетативной дистонии становятся дети с высоким исходным тонусом и легкой либо острой недостаточностью симпатического отдела.
Пролапс митрального клапана часто сочетается со стигмами дизэмбриогенеза (незначительные аномалии развития). Чаще всего это указывает на некую неполноценность вегетативной дистонии, а также соединительной ткани.
Вегетативная дистония в сочетании с артериальной гипертензией характеризуется увеличением артериального давления. Это достаточно популярное отклонение, которое нередко перерастает в гипертонию различных степеней. Симптоматика данного отклонения следующая: ухудшение памяти, кардиалгия, раздражительность, чрезмерная утомляемость, головокружения и частые головные боли. Что касается головной боли, она одолевает затылочно-теменную или затылочную зону и имеет монотонный давящий характер. Она появляется после пробуждения или днем и способна усиливаться после определенных нагрузок. Зачастую к головным болям добавляется еще один симптом – тошнота, но до рвоты дело не доходит.
Вегетативная дистония, сочетающаяся с артериальной гипертензией проявляется уже в 7-9 лет. Как правило, она влияет на пульсовое давление, которое опускается до отметки в 30-35 мм ртутного столба. Головные боли при данном заболевании можно легко притупить при помощи перерыва в учебе или отдыхе от физических нагрузок, полноценного здорового сна, пеших прогулок на свежем воздухе.
При данном заболевании отмечается ухудшенное физическое развитие детей. Степень этого отставания зависит исключительно от степени самого заболевания. Чаще всего дети, страдающие вегетативной дистонией с артериальной гипертензией, имеют бледную кожу, красный дермографизм и ярко выраженную сосудистую сетку.
Что происходит?
Недостаточно количество сурфактанта в легких недоношенного ребенка приводит к тому, что на выдохе лёгкие как бы захлопываются (спадаются) и ребёнку приходится при каждом вдохе их заново раздувать. Это требует больших затрат энергии, в результате силы новорожденного истощаются и развивается тяжёлая дыхательная недостаточность. В 1959 году американскими учеными М.Е. Avery и J. Mead была обнаружена недостаточность легочного сурфактанта у недоношенных новорожденных детей, страдающих респираторным дистресс-синдромом, таким образом и была установлена основная причина РДС. Частота развития РДС тем выше, чем меньше срок, на котором родился ребенок. Так, им страдают в среднем 60 процентов детей, родившихся при сроке беременности менее 28 недель, 15—20 процентов — при сроке 32—36 недель и всего 5 процентов — при сроке 37 недель и более.
Клиническая картина синдрома проявляется, прежде всего, симптомами дыхательной недостаточности, развивающимися, как правило, при рождении, или через 2-8 часов после родов — учащение дыхания, раздувание крыльев носа, втяжение межреберных промежутков, участие в акте дыхания вспомогательной дыхательной мускулатуры, развитие синюшности (цианоза). Из-за недостаточной вентиляции легких очень часто присоединяется вторичная инфекция, и пневмония у таких младенцев — отнюдь не редкость. Естественный процесс выздоровления начинается после 48-72 часов жизни, однако не у всех детей этот процесс идёт достаточно быстро — из-за развития упомянутых уже инфекционных осложнений.
При рациональном выхаживании и тщательном соблюдении протоколов лечения детей с РДС выживает до 90 процентов маленьких пациентов. Перенесенный респираторный дистресс-синдром в дальнейшем практически не отражается на состоянии здоровья детей.
Источники
- Glaser K., Wright CJ. Indications for and Risks of Noninvasive Respiratory Support. // Neonatology — 2021 — Vol — NNULL — p.1-9; PMID:33902052
- Sirisangwon R., Phupong V. Vaginal Progesterone Supplementation in the Management of Preterm Labor: A Randomized Controlled Trial. // Matern Child Health J — 2021 — Vol — NNULL — p.; PMID:33900515
- Stomnaroska O., Kocovski G., Zdravkovski P., Ilievski B., Jovanovic R., Petrusevska G. Large Neck Teratoma in a Newborn with Respiratory Distress Syndrome. // Pril (Makedon Akad Nauk Umet Odd Med Nauki) — 2021 — Vol42 — N1 — p.105-108; PMID:33894120
- Picón-César MJ., Molina-Vega M., Suárez-Arana M., González-Mesa E., Sola-Moyano AP., Roldan-López R., Romero-Narbona F., Olveira-Fuster G., Tinahones FJ., González-Romero S. MeDiGes Study. Metformin versus insulin in gestational diabetes: Glycemic control, and obstetrical and perinatal outcomes. Randomized prospective trial. // Am J Obstet Gynecol — 2021 — Vol — NNULL — p.; PMID:33887240
- Pokutnaya D., Shirzadi MR., Salari E., Molaei G. Cutaneous Leishmaniasis during Pregnancy, Preterm Birth, and Neonatal Death: A Case Report. // Iran J Parasitol — 2021 — Vol15 — N4 — p.608-614; PMID:33884019
- Dell’Edera D., Allegretti A., Forte F., Dell’Edera RA., Dell’Edera MT., Epifania AA., Mercuri L., Catacchio CR., Mitidieri A., Simone F., Ventura M. 7q35q36.3 deletion and concomitant 20q13.2q13.33 duplication in a newborn: familiar case. // Eur Rev Med Pharmacol Sci — 2021 — Vol25 — N7 — p.2949-2957; PMID:33877658
- Paes LS., Carvalho FH., Araujo Júnior E., Feitosa HN. Assessment of morbidity and mortality in newborns with late prematurity: experience of a reference maternity in the northeast of Brazil. // Minerva Obstet Gynecol — 2021 — Vol — NNULL — p.; PMID:33876899
- Gunes AO., Karadag N., Cakir H., Toptan HH., Karatekin G. The Associations Between Lung Ultrasonography Scores in the First Day of Life and Clinical Outcomes. // J Ultrasound Med — 2021 — Vol — NNULL — p.; PMID:33871883
- Zuiki M., Kume R., Matsuura A., Mitsuno K., Kitamura K., Kanayama T., Komatsu H. Large difference between Enghoff and Bohr dead space in ventilated infants with hypoxemic respiratory failure. // Pediatr Pulmonol — 2021 — Vol — NNULL — p.; PMID:33866691
- Bartal MF., Ward C., Blackwell SC., Ashby Cornthwaite JA., Zhang C., Refuerzo JS., Pedroza C., Lee KH., Chauhan SP., Sibai BM. Detemir versus Neutral Protamine Hagedorn Insulin for Diabetes Mellitus in Pregnancy: A Comparative-Effectiveness, Randomized Controlled Trial. // Am J Obstet Gynecol — 2021 — Vol — NNULL — p.; PMID:33865836
Что значит SDR?
Одним из основных показателей прочностных характеристик полиэтиленовой трубы, который предусмотрен ГОСТом и обязательно указывается при маркировке, является SDR. Этот параметр позволяет определить возможности изделий. Расшифровка этого обозначения на английском (Standart Dimension Ratio) – стандартный размерный коэффициент.
Коэффициент SDR трубы показывает соотношение внешнего ее диаметра к толщине стенки, для вычисления показателя применяется следующая формула:
SDR = D : S, где D – наружный диаметр (в мм), а S – толщина стенки трубы (в мм).
Чем больше коэффициент SDR, тем тоньше трубная стенка, и наоборот – у трубы с толстыми стенками этот показатель меньше. Таким образом, труба с низким SDR будет обладать большими возможностями и способностью выдерживать серьезные нагрузки, чем изделие с высоким коэффициентом.
Важно! Если из труб одного диаметра и с разными показателями SDR (например, 17 и 21) выбирать изделие с лучшими эксплуатационными характеристиками, следует отдать предпочтение меньшему коэффициенту– 17.Однако нужно учитывать: чем больше толщина стенки, тем ниже пропускная способность трубы за счет уменьшения ее внутреннего сечения
Причины хронической ишемии головного мозга
К главным причинам хронической ишемии головного мозга относят артериальную гипертензию и атеросклероз. Часто встречается хроническая ишемия головного мозга, вызванная сочетанием двух состояний. Кроме того, среди других причин, обусловливающих данное заболевание, будут симптомы сердечно-сосудистых заболеваний, которые выражаются в нарушении сердечного ритма (например, в аритмии), что, в свою очередь, приводит к снижению системного типа гемодинамики.
Большое значение врачи отводят исследованию и аномалии сосудов, как головного мозга, так и сосудов шейного отдела. Такие аномалии, как и те, что связаны с аортой или сосудами плечевого пояса, часто долго не проявляют себя, вплоть до момента развития атеросклеротических и гипертонических процессов.
В последние годы врачи-неврологи выделяют и ряд других причин, способствующих развитию хронической ишемии головного мозга, среди которых венозная патология интракраниального и экстракраниального характера. Не исключено, что на возникновение хронической ишемии влияет компрессия артериальных и венозных сосудов
Врачи берут во внимание как спондилогенное влияние, так и возможное сдавливание сосудов мышцами, аневризмой или опухолью. Еще одна возможная причина данной патологии — развивающийся церебральный амилоидоз
Обычно выявленная энцефалопатия симптоматически проявляет себя смешано. Если были обнаружены факторы, обусловившие развитие хронической ишемии головного мозга, то все другие возможные причины отходят в плоскость дополнительных причин. Безусловно, обнаружить и точно определить дополнительные факторы, которые усугубляют протекание заболевания, будет весьма необходимым, в первую очередь, чтобы принять правильное решение касательно симптоматического или этиопатогенетического лечения.
В медицине последних лет возникновение хронической ишемии головного мозга принято рассматривать в двух вариантах: по характеру и природе повреждения и по привычной локализации. В случае двустороннего диффузного поражения головного мозга, точнее, его белого вещества, говорят о лейкоэнцефалопатической разновидности энцефалопатии. Вторым вариантом является лакунарный тип, имеющий большое число лакунарных очагов. Если такие два варианта чаще всего встречаются в теории, то на практике говорят об их смешанном типе.
Чаще всего лакунарный вариант вызывается таким процессом, как окклюзия мелких сосудов. Значительную роль в патогенезе диффузного поражения отводят снижению системной гемодинамики или, как ее еще называют, артериальной гипотензии. Причиной снижения артериального давления будет неправильно проведенная антигипертензивная терапия, а также понижение сердечного сброса. Значительная роль отводится сильному кашлю, ортостатической гипотензии, что бывает часто в случае вегето-сосудистой дистонии.
Как известно, главным патогенетическим звеном данного заболевания является истощение механизма компенсации, а также снижение энергетической работы мозга, что приводит к явному развитию функциональных расстройств и таким необратимым процессам морфологического характера, как замедление кровотока, понижение уровня глюкозы в крови, снижение уровня кислорода, возникновение капиллярного стаза, появление замедленного мозгового кровотока, тромбообразование, способность к деполяризации клеточных мембран.
Профилактика
Специфическая профилактика ОРДС у взрослых отсутствует. Среди общих рекомендаций — минимизация риска воздействия повреждающих стрессовых факторов (травм грудной клетки, своевременное/адекватное лечение инфекционных заболеваний легких и др.).
В основе профилактики СДР у новорожденных — профилактика невынашивания беременности (преждевременных родов). Из медикаментозных средств при угрозе преждевременных родов следует проводить терапию, стимулирующую процесс созревания у плода легочной ткани (бетаметазон, дексаметазон, эуфиллин, тироксин). Детям, родившимся недоношенными, проводится ранняя заместительная терапия сурфактантом (в первые часы после рождения).
О статье.
Данная статья продолжает цикл публикаций на нашем сайте, посвященный применению лекарств во время беременности. Использованы материалы методических рекомендаций Британской Королевской Коллегии Акушеров и Гинекологов.
Одна из самых частых причин высокой смертности недоношенных детей — развитие респираторного дистресс синдрома. Введение ГК до начала преждевременных родов, когда полностью предотвратить их невозможно, позволяет снизить риск возникновения этого серьезного расстройства. Антенатальное (дородовое) введение ГК значительно повышает эффективность реанимационных и лечебных мероприятий, которые сохраняют жизнь новорожденному. Респираторный дистресс синдром новорожденных РДС (болезнь гиалиновых мембран) — дыхательное расстройство, поражающее в первую очередь недоношенных детей, родившихся до полного биохимического созревания легких.
Важное событие внутриутробного развития легких — синтез и секреция сурфактанта альвеоцитами II типа (специальные клетки, выстилающие изнутри альвеолы). Альвеолы — это своеобразные «мешочки», которыми заканчивается разветвление бронхиального дерева
Именно в альвеолах происходит газообмен между вдыхаемым воздухом и кровью. Основная функция сурфактанта — снижение сил поверхностного натяжения альвеол и повышение эластичности легочной ткани. Сурфактант предотвращает спадение и «склеивание» альвеол в конце выдоха. Если альвеолы «склеиваются», они уже не участвуют в газообмене, и в организме развивается гипоксия (недостаточность кислорода в тканях, в первую очередь в центральных органах жизнеобеспечения — головном мозге, почках, надпочечниках). В сурфактанте в значительном количестве содержатся фосфолипиды (лецитин, сфингомиелин, фосфотидилхолин, фосфотидилглицерин). По соотношению лецитина к сфингомиелину в амниотической жидкости косвенно можно судить о количестве внутриальвеолярного сурфактанта и степени зрелости легких.
На образование сурфактанта и созревание легких плода может влиять много факторов, например, повышение уровня глюкозы и инсулина в крови плода при нарушениях углеводного обмена у матери (сахарный диабет, диабет беременных). Кстати прием ГК предрасполагает к развитию гиперинсулинемиии и гипергликемии в крови и матери, и плода.
У недоношенных детей, вследствие недостатка сурфактанта в альвеолах, легкие плохо расправляются, что приводит к ателектазу (спадению легочной ткани) и нарушению дыхания вплоть до развития тяжелых дыхательных расстройств. При соответствующем лечении исход, как правило, благоприятен. Однако, у глубоконедоношенных детей РДС сопровождается высокой смертностью
Вот почему во всем мире уделяется большое внимание вопросам лечения РДС
Важно отметить, что введение сурфактанта недоношенным детям значительно улучшает их состояние и выживаемость. Но этот вид лечения является достаточно дорогостоящим для национальных систем здравоохранения, поэтому важное внимание уделяют вопросам профилактики развития РДС новорожденных, родившихся раньше срока.
Но этот вид лечения является достаточно дорогостоящим для национальных систем здравоохранения, поэтому важное внимание уделяют вопросам профилактики развития РДС новорожденных, родившихся раньше срока.
Сравнительный анализ эффективности различных препаратов сурфактанта
Различные природные препараты сурфактанта изу чались в рандомизированных клинических исследованиях, которые в 2015 г. были обобщены в систематизированном обзоре и мета-анализе, выполненном экспертами Cochrane . В мета-анализ вклю чали клинические исследования, в которых изучалась эффективность профилактического и лечебного применения сурфактанта, соответственно, у недоношенных детей (менее 32 недель гестации) с угрозой развития РДСН и недоношенных детей (менее 37 недель гестации), у которых имелись клинические и рентгенологические признаки РДСН. Первичными конечными точками были неонатальная летальность (в возрасте до 28 дней), госпитальная летальность и хроническое поражение легких (необходимость в оксигенотерапии в возрасте 28-30 дней или постменструальном возрасте 36 недель). Кроме того, оценивали различные вторичные конечные точки, включая дозы сурфактанта, пневмоторакс, легочное кровотечение, открытый артериальный проток и др. В целом в мета-анализ были включены 16 рандомизированных клинических исследований.
Сравнение препаратов сурфактанта, выделенных из лаважной жидкости (калфактант или бовактант) или ткани легких (берактант или сурфактант ТА) телят. Эффективность различных препаратов бычьего сурфактанта сравнивали в 9 исследованиях (профилактика – 2, лечение – 7)
Достоверной разницы частоты неблагоприятных исходов между группами сравнения выявлено не было, в частности риск смерти или развития хро нического поражения легких не отличался при при менении различных бычьих сурфактантов как с профилактической (относительный риск 1,02; 95% доверительный интервал 0,89-1,17; n=1123), так и с лечебной целью (ОР 0,95; 95% ДИ 0,86-1,07; n=2009). Риск отдельных первичных и вторичных конечных точек также был сопоставимым при назначении препаратов сурфактанта, выделенных из лаважной жидкости или ткани легких телят.
Сравнение препаратов сурфактанта, выделенных из ткани легких телят (берактант или сурфактант ТА) или свиней (порактант альфа). Сравнительных исследований профилактической эффективности бычьего и свиного сурфактантов авторы не выявили, однако в 9 исследованиях сравнивали эффективность их лечебного применения у недоношенных детей с РДСН. В этих исследованиях введение берактанта ассоциировалось с более высоким риском госпитальной смертности (ОР 1,44, 95% ДИ 1,04-2,00; n=901, рис. 1), смерти или потребности в кислороде в постменструальном возрасте 36 недель (ОР 1,30, 95% ДИ 1,04-1,64; n=448) и открытого артериального протока, потребовавшего лечения (ОР 1,86, 95% ДИ 1,28-2,70). Вероятность введения более одной дозы препарата также была выше при применении бычьего сурфактанта (ОР 1,57, 95% ДИ 1,291,92). Частота других конечных точек достоверно не отличалась между группами сравнения. При анализе подгрупп, выделенных с учетом стартовой дозы сурфактанта, преимущества порактанта альфа перед берактантом были выявлены только у детей, которым свиной сурфактант вводили в более высокой стартовой дозе (>100 мг/кг). В этой выборке при применении берактанта отмечалось достоверное увеличение риска смерти перед выпиской (ОР 1,62, 95% ДИ 1,11-2,38) и смерти или потребности в кислороде в постменструальном возрасте 36 недель (ОР 1,39, 95% ДИ 1,08-1,79) по сравнению с таковым у детей, получавших порактант альфа.
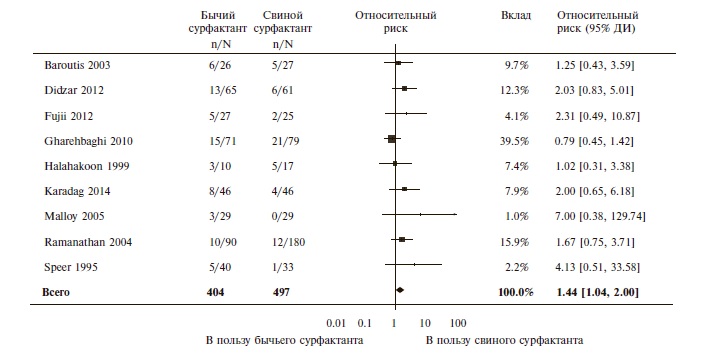 Рис. 1. Относительный риск смерти передвыпиской при применении сурфактантов, полученных из легких телят и свиней
Рис. 1. Относительный риск смерти передвыпиской при применении сурфактантов, полученных из легких телят и свиней
Профилактика
Проводятся мероприятия по антенатальной охране ребенка, в том числе: борьба с токсикозами беременных, предупреждение недонашивания, внутриутробной гипоксии, асфиксии, внутриутробной инфекции.
Библиография: Кравцов В. И. Реанимация и лечение дыхательной недостаточности новорожденных в условиях гипербарической оксигенации, Вопр. охр. мат. и дет., т. 17, № 7, с. 45, 1972; Панов Н. А. Рентгенологические аспекты пневмопатий у новорожденных детей, Педиатрия, № 6, с. 39, 1974; Слепых А. С., Костин Э. Д. и Кучинский Ю. П. Лечение новорожденных, имеющих нарушение функции внешнего дыхания, кислородно-гелиевыми смесями в условиях повышенного давления, Вопр. охр. мат. и дет., т. 19, № 7, с. 33, 1974; Сморчков А. П. Синдром дыхательных расстройств у новорожденных детей, Педиатрия, № 6, с. 80, 1974, библиогр.; Сотникова К. А., Буракова В. Б. и Поддубная А. Е. Синдром дыхательных расстройств у детей первых дней жизни, Вопр, охр. мат. и дет., т. 20, N» 5, с. 46, 1975, библиогр.; Ballard R. А. а. о. Idiopatic respiratory distress syndrome, Amer. J. Dis. Child., v. 125, p. 676, 1973, bibliogr.; Favara B., Franciosi R. A. a. Butterfield L. J. Disseminated intravascular and cardiac thrombosis of the neonate, ibid., v. 127, p. 197, 1974; Lallemand D. et Sauvergrain J. Diagnostic radiologique des detresses respkatoires neonatales, Rev. Pediat., t. 10, p. 395, 1974; Outerbridge E. W. a. o. Idiopathic respiratory distress syndrome, Amer. J. Dis. Child., v. 123, p. 99, 1972.