В основе геморрагического шока лежит:
Содержание:
Клиническая классификация
Действия медицинского персонала, необходимая помощь при геморрагическом шоке в акушерстве находятся в прямой зависимости от стадии его развития, или, другими словами, степени тяжести. Существует классификация, основанная на снижении показателя объема циркулирующей крови (ОЦК). Снижение на 20% определяется как шок легкой степени, на 35-40% — средней степени, на 40% и более — тяжелой степени. В этих случаях особое значение приобретает скорость потери крови.
Еще одна классификация основана на определении шокового индекса Альговера, который в норме должен быть меньше 1 (единицы). Он определяется путем деления числа сердечных сокращений на систолический показатель артериального давления. Стадия, или степень шока, определяется как легкая при индексе от 1 до 1,1, средняя — 1,5, тяжелая —2, крайне тяжелая — 2,5.
В практических целях для определения тяжести состояния пациентки и решения вопроса о том, какая неотложная помощь именно в данном конкретном случае должна быть оказана, используются перечисленные показатели с учетом клинико-лабораторных данных.
При этом различают следующие стадии геморрагического шока:
- I стадия (легкая) — компенсированный шок;
- II стадия (средняя) — декомпенсированный обратимый;
- III стадия (тяжелая) — декомпенсированный необратимый, или терминальный.
Рассмотрим их более подробно.
I стадия
Соответствует периоду кризиса макроциркуляции и представляет собой стадию централизации кровообращения. Ее развитие происходит при кровопотере, которая не превышает 20% объема циркулирующей крови, что составляет приблизительно 1 л. Индекс Альговера составляет от 0,5 и выше.
Среди клинической симптоматики преобладают признаки изменения функциональных нарушений деятельности сердечно-сосудистой системы. К ним относятся «запустение» периферических вен конечностей, бледность кожных покровов и слизистых оболочек, умеренное повышение как систолического, так и диастолического артериального давления, иногда их незначительное снижение, умеренное увеличение числа сердечных сокращений (до 100-110), незначительное увеличение частоты дыхания (до 20 в 1 мин.), возможно незначительное снижение диуреза.
II стадия
Характеризуется углублением расстройства кровообращения и нарастающим истощением компенсаторно-приспособительных механизмов. Она соответствует кризису микроциркуляции и развивается при среднем дефиците объема циркулирующей крови 35% (20-40%). При этом объем кровопотери составляет около 1-2 л, а индекс Альговера достигает 1,5 и выше.
Клиническая симптоматика имеет тенденцию к дальнейшему ухудшению: на фоне беспокойства, повышенной возбудимости, бледности кожных покровов появляются акроцианоз (цианотичность губ, ногтей, мочек ушей), холодный пот, одышка до 24-30 дыханий в 1 мин., систолическое артериальной давление снижается до 100-90 мм. рт. ст., а диастолическое — остается незначительно повышенным, число сердечных сокращений достигает 120 в 1 мин., диурез уменьшается до 20-30 мл в 1 час. Появляются соответствующие изменения на ЭКГ, снижается центральное венозное давление, в анализе крови отмечаются незначительное снижение гемоглобина, уменьшение числа эритроцитов (до 3 х 1012/л), гематокрита.
Кроме того, возможно появление признаков нарушения свертываемости крови — отсутствие свертывания вытекающей из матки крови, рвота содержимым желудка, имеющим коричневатую окраску (цвет «кофейной гущи»), кровоизлияния на слизистых оболочках и кожных покровах (в местах инъекций, кожных складок и т. д.).
III стадия
Представляет собой терминальную фазу кризиса гемостатической системы, необратимое состояние нарушения компенсаторно-приспособительных механизмов организма. Она развивается при дефиците объема циркулирующей крови свыше 40%, что составляет около 2 л кровопотери при шоковом индексе 2 и выше.
Отмечается психомоторное возбуждение и спутанность сознания, позже развиваются сонливость и кома. Кожные покровы холодные, бледные с выраженной «мраморностью», температура тела на 2-3 градуса ниже нормы. Одышка увеличивается до 30-40 в 1 мин и более, возможно нарушение ритма дыхания. Частота сердечных сокращений превышает 120-140 в 1 мин. Центральное венозное давление резко снижено или отрицательное, но при развитии сердечной недостаточности, наоборот, оно выше нормы и даже высокое. Число эритроцитов в анализе крови не превышает 2,5 х 1012/л, гематокрит достигает 25% и меньше, мочеотделение от 15 до 5 мл в 1 час вплоть до ее полного отсутствия, отмечается развитие ДВС-синдрома.
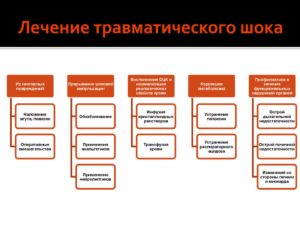
Лечение геморрагического шока
Лечение геморрагического шока чрезвычайно ответственная задача, для решения которой врач-гинеколог должен объединить усилия с анестезиологом-реаниматологом, а в случае необходимости – привлечь гематолога-коагулолога.
Для обеспечения успеха терапии необходимо руководствоваться следующим правилом: лечение должно начинаться как можно раньше, быть комплексным, проводиться с учетом причины, вызвавшей кровотечение, и состояния здоровья больной, предшествовавшего ему.
Комплекс лечебных мероприятий включает в себя следующее:
- Гинекологические операции по остановке кровотечения.
- Оказание анестезиологического пособия.
- Непосредственное выведение больной из состояния шока.
Все перечисленные мероприятия должны осуществляться параллельно, четко и быстро.
От каких механизмов зависит тяжесть шока?
В развитии патогенеза компенсации кровопотери имеют значение:
- состояние нервной регуляции сосудистого тонуса;
- способность сердца работать в условиях гипоксии;
- свертываемость крови;
- условия окружающей среды по дополнительному обеспечению кислородом;
- уровень иммунитета.
Ясно, что у человека с хроническими заболеваниями шансов перенести массивную кровопотерю значительно меньше, чем у ранее здорового. Работа военных медиков в условиях афганской войны показала, насколько тяжелой оказывается умеренная кровопотеря для здоровых бойцов в условиях высокогорья, где насыщенность воздуха кислородом снижена.
Быстрая транспортировка раненых с помощью БТР-ов и вертолетов спасла немало солдат
У человека в среднем циркулирует постоянно около 5л крови по артериальным и венозным сосудам. При этом 75% находится в венозной системе. Поэтому от быстроты адаптации именно вен зависит последующая реакция.
Внезапная потеря 1/10 части от циркулирующей массы не дает возможности быстро «пополнить» запасы из депо. Венозное давление падает, что ведет к максимальной централизации кровообращения для поддержки работы самого сердца, легких и головного мозга. Такие ткани, как мышцы, кожа, кишечник организмом признаются «лишними» и выключаются из кровоснабжения.
Во время систолического сокращения выталкиваемый объем крови недостаточен для тканей и внутренних органов, он питает только коронарные артерии. В ответ включается эндокринная защита в виде повышенной секреции адренокортикотропного и антидиуретического гормонов, альдостерона, ренина. Это позволяет задержать жидкость в организме, прекратить мочевыделительную функцию почек.
Одновременно повышается концентрация натрия, хлоридов, но теряется калий.
Повышенный синтез катехоламинов сопровождается спазмом сосудов на периферии, растет сосудистое сопротивление.
За счет циркуляторной гипоксии тканей наступает «закисление» крови накопившимися шлаками — метаболический ацидоз. Он способствует нарастанию концентрации кининов, которые разрушают сосудистые стенки. Жидкая часть крови выходит в межтканевое пространство, а в сосудах накапливаются клеточные элементы, образуются все условия для повышенного тромбообразования. Возникает опасность необратимого диссеминированного внутрисосудистого свертывания (ДВС-синдрома).
Сердце пытается компенсировать необходимый выброс учащением сокращений (тахикардией), но их не хватает. Потери калия снижают сократительную способность миокарда, формируется сердечная недостаточность. Артериальное давление резко падает.
Восполнение объема циркулирующей крови способно предотвратить общие нарушения микроциркуляции. От скорости и полноты оказания мероприятий неотложного значения зависит жизнь пациента.
Признаки геморрагического шока
Из-за патологического нарушения микроциркуляции крови происходит нарушение своевременного поступления в ткани кислорода, энергетических продуктов и питательных веществ. Наступает кислородное голодание, которое максимально быстро нарастает в легочной системе, из-за чего учащается дыхание, появляется одышка и возбуждение. Компенсаторное перераспределение крови приводит к уменьшению ее количества в мышцах, на что может указывать бледность кожи, холодные и влажные конечности.
Наряду с этим происходит метаболический ацидоз, когда происходит повышение вязкости крови, которая постепенно закисляется накопившимися шлаками. На разных стадиях шок может сопровождаться другими признаками, такими как:
- тошнота, сухость во рту;
- сильное головокружение и слабость;
- тахикардия;
- уменьшение почечного кровотока, что проявляется гипоксией, некрозом канальцев и ишемией;
- потемнение в глазах, потеря сознания;
- снижение систолического и венозного давления;
- запустение подкожных вен на руках.
Симптомы
Клиническая картина геморрагического шока развивается в соответствии с его стадиями. Клинически на первый план выступают признаки кровопотери. На стадии компенсированного геморрагического шока сознание, как правило, не страдает, больной отмечает слабость, может быть несколько возбужденным или спокойным, кожные покровы бледные, на ощупь — холодные конечности.
Важнейшим симптомом на этой стадии является запустевание подкожных венозных сосудов на руках, которые уменьшаются в объеме и становятся нитевидными. Пульс слабого наполнения, учащенный. Артериальное давление, как правило, нормальное, иногда повышенное. Периферическая компенсаторная вазоконстрикция обусловлена гиперпродукцией катехоламинов и возникает практически немедленно после кровопотери. На этом фоне, одновременно у пациента развивается олигурия. При этом, количество выделяемой мочи может снижаться наполовину и даже более. Резко снижается центральное венозное давление, что обусловлено уменьшением венозного возврата. При компенсированном шоке ацидоз чаще отсутствует или носит локальный характер и слабо выражен.
На стадии обратимого декомпенсированного шока признаки расстройств кровообращения продолжают углубляться. В клинической картине, для которой характерны признаки компенсированной стадии шока (гиповолемия, бледность, обильный холодный и липкий пот, тахикардия, олигурия) в качестве основного кардинального симптома выступает гипотония, что свидетельствует о расстройстве механизма компенсации кровообращения. Именно в стадии декомпенсации начинаются нарушения органного (в кишечнике, печени, почках, сердце, головном мозге) кровообращения. Олигурия, которая в стадии компенсации развивается вследствии компенсаторных функций, на этой стадии возникает на базе снижения гидростатического давления крови и расстройств почечного кровотока.
На этой стадии проявляется классическая клиническая картина шока: акроцианоз и похолодание конечностей, усиление тахикардии и появление одышки, глухость сердечных тонов, что свидетельствует об ухудшении сократимости миокарда. В ряде случаев отмечается выпадение отдельных/целой группы пульсовых толчков на периферических артериях и исчезновение при глубоком вдохе тонов сердца, что свидетельствует об крайне низком венозном возврате.
Больной заторможен или находится в состоянии прострации. Развивается одышка, анурия. Диагностируются ДВС-синдром. На фоне максимально выраженной вазоконстрикции периферических сосудов происходит прямой сброс в венозную систему артериальной крови через открывающиеся артериовенозные шунты, что позволяет повысить насыщение кислородом венозной крови. На этой стадии выражен ацидоз, являющийся следствием нарастающей тканевой гипоксии.
Стадия необратимого шока качественно не отличается от декомпенсированного шока, но является стадией ещё более выраженных и глубоких нарушений. Развитие состояния необратимости проявляется вопросом времени и определяется накоплением токсических веществ, гибелью клеточных структур, появлением признаков полиорганной недостаточности. Как правило, на этой стадии отсутствует сознание, пульс на периферийных сосудах практически не определяется, АД (систолическое) на уровне 60 мм рт. ст. и ниже, с трудом определяется, ЧСС на уровне 140/мин., дыхание ослаблено, ритм нарушен, анурия. Эффект от инфузионно-трансфузнонной терапии отсутствует. Длительность этой стадии составляет 12-15 часов и завершается летальным исходом.
Диагностика геморрагического синдрома
Вовремя установленный диагноз поможет специалисту назначить эффективное лечение, а вам – сделать свои сосуды здоровыми раз и навсегда. Подтвердить или опровергнуть диагноз можно, сдав ряд лабораторных анализов, направленных на получение детальной информации о состоянии крови. Также понадобится провести коагуляционные тесты, во время спорных ситуаций врач-диагност может взять стернальную пункцию для углубленной диагностики.
После получения полной картины заболевания, определения ее стадии, причин и степени тяжести геморрагического синдрома, будет назначено лечение.
Лечение геморрагического синдрома
Основой выбора метода лечения геморрагического синдрома является определение причины заболевания, однако существуют следующие ключевые принципы:
- Вне зависимости от причины, пациенту оказывается неотложная медицинская помощь, которая остановит кровотечение. Для этого применяют викасол, хлорид кальция, витамин С, а также раствор тромбопластина.
- В случае возникновения патологии на фоне приема сильнодействующих лекарственных препаратов, их отмена является обязательной.
- Местная терапия геморрагий осуществляется с помощью сухого тромбина, гомеостатических губок, аминометилбензойной кислоты (Амбен).
- При обильных кровопотерях может быть необходима трансфузия крови или ее фракций, предпочтительно напрямую от донора.
- Также при геморрагическом синдроме различной этиологии применяются препараты серотонина, например, Динатон.
Профилактика геморрагического синдрома
Важнейшей и основополагающей частью предупреждения геморрагического синдрома является полное медицинское обследование для своевременного установления и устранения его возможных причин.
Новорожденным недоношенным детям необходимо введение подкожно витамина К и прикладывание ребенка к груди как можно скорее после рождения.
Диетическое питание пациентов, склонных в данной патологии, должно быть основано на усиленном потреблении витамина К, а также белков, овощей и фруктов. Кроме того, таким людям необходимо избегать физической активности, приводящей к возникновению травм и ранений.
Так же вас может заинтересовать
Геморрагический шок: степени, классификация
Как же определяется степень кровопотери, ведь для адекватной и эффективной терапии шоковых состояний, связанных потерей части крови, важно точно и своевременно определить степень кровопотери. На сегодняшний день из всех возможных классификаций острой кровопотери, практическое применение получила такая:
На сегодняшний день из всех возможных классификаций острой кровопотери, практическое применение получила такая:
- легкая степень (потеря крови от 10% до 20% объема крови), не превышающая 1 литр;
- средняя степень (кровопотеря от 20% до 30% объема крови), в пределах до 1,5 литров;
- тяжелая степень (кровопотеря порядка 40% объема крови), достигающая 2 литров;
- крайне тяжелая, или массивная кровопотеря — когда теряется свыше 40% объема крови, составляя более 2 литров.
В отдельных случаях интенсивной кровопотери развиваются нарушения гомеостаза необратимого характера, не поддающиеся коррекции даже моментальным восполнением объема крови.
Потенциально смертельными считают следующие виды кровопотери:
- потеря в течение суток 100% объема циркулирующей крови (далее – ОЦК);
- потеря в течение 3 часов 50% ОЦК;
- одномоментная потеря 25% объема ЦК (1,5-2 литров);
- форсированная потеря крови со скоростью 150 мл в минуту.
Для определения степени кровопотери и степени тяжести геморрагического шока используется комплексная оценка клинических, параклинических и гемодинамических показателей.
Шоковый индекс Альговера
Большое значение имеет подсчет шокового индекса Альговера, определяемого как частное при делении показателя частоты сердечных сокращений на величину систолического давления. В норме шоковый индекс составляет менее 1. В зависимости от степени кровопотери и тяжести шока это может быть:
- индекс от 1 до 1,1 соответствующий легкой степени кровопотери;
- индекс 1, 5 — средней степени кровопотери;
- индекс 2 — тяжелой степени кровопотери;
- индекс 2,5 — крайне тяжелой степени кровопотери.
Кроме индекса Альговера, уточнению объема потерянной крови помогает измерение величины артериального и центрального венозного давления (АД и ЦВД), мониторирование минутного или почасового диуреза, а также уровень гемоглобина крови и его соотношение с показателем гематокрита (удельного веса эритроцитарной массы от общего объема крови).
О легкой степени кровопотери говорят следующие признаки:
- Частота сердечных сокращений менее 100 ударов в минуту, бледность,
- сухость и пониженная температура кожных покровов,
- величина гематокрита от 38 до 32 %, ЦВД от 3 до 6 мм водного столба,
- величина диуреза более 30 мл.
Кровопотеря средней степени проявляется более выраженными симптомами:
- Учащением ЧСС до 120 ударов в минуту,
- возбуждением и беспокойным поведением,
- появлением холодного пота,
- падением ЦВД до 3-4 см водного столба,
- снижением гематокрита до 22-30%,
- диурезом менее 30 мл.
О тяжелой степени кровопотери свидетельствуют:
- Тахикардия более 120 в минуту,
- падение артериального давления ниже 70 мм рт. ст., а венозного — меньше 3 мм вод ст.,
- выраженная бледность кожи, сопровождаемая липким потом,
- анурия (отсутствие мочи),
- понижение гематокрита ниже 22%, гемоглобина — менее 70 г/л.
Патогенез
К основным факторам развития геморрагического шока относятся:
- Выраженный дефицит ОЦК с развитием гиповолемии, что приводит к снижению сердечного выброса.
- Снижение кислородной ёмкости крови (уменьшается доставка кислорода к клеткам и обратная транспортировка углекислого газа. Также страдает процесс доставки питательных веществ и вывода продуктов метаболизма).
- Нарушения гемокоагуляции, вызывающие расстройства в микроциркуляторном сосудистом русле — резкое ухудшение реологических свойств крови — повышения вязкости (сгущение), активизация свертывающей системы крови, агглютинация форменных элементов крови и др.
Как следствие возникает гипоксия, чаще смешанного типа, капилляротрофическая недостаточность, обуславливающая нарушения функции органов/тканей и расстройство жизнедеятельности организма. На фоне нарушения системной гемодинамики и уменьшения интенсивности биологического окисления в клетках включаются (активизируются) адаптационные механизмы, направленные на поддержание жизнедеятельности организма.
Механизмы адаптации прежде всего включают в себя вазоконстрикцию (сужение сосудов), которая возникает из-за активации симпатического звена нейрорегуляции (выделение адреналина, норадреналина) и действия гуморально-гормональных факторов (глкокортикоиды, антидиуретический гормон, АКТТ и т.д.).
Вазоспазм способствует уменьшению ёмкости сосудистого кровеносного русла и централизации процесса кровообращения, что проявляется снижением объёмной скорости кровотока в печени, почках, кишечнике и сосудах нижних/верхних конечностей и создаёт предпосылки в дальнейшем для нарушения функции этих систем и органов. В тоже время, кровоснабжение головного мозга, сердца, лёгких и мышц, участвующих в акте дыхания, продолжает сохраняться на достаточном уровне и нарушается в самую последнюю очередь.
Этот механизм без выраженной активации других механизмов компенсации у здорового человека способен самостоятельно нивелировать утрату около 10–15% ОЦК.
Развитие выраженной ишемии большого тканевого массива способствует накоплению в организме недоокисленных продуктов, нарушениям в системе энергообеспечения и развитию анаэробного метаболизма. В качестве адаптационной реакции на прогрессирующий метаболический ацидоз можно считать усиление катаболических процессов, поскольку они способствует более полной утилизации кислорода различными тканями.
К относительно медленно развивающимся адаптивным реакциям относится перераспределение жидкости (её перемещение в сосудистый сектора из интерстициального пространства). Однако, такой механизм реализуется только в случаях медленно происходящего незначительного кровотечения. К менее эффективным приспособительным реакциям относятся увеличение частоты сердечных сокращений (ЧСС) и тахипноэ.
Развивающаяся сердечная/дыхательная недостаточность является ведущей в патогенезе острой кровопотери. Объемное кровотечение приводит к децентрализации системного кровообращения, запредельному снижению кислородной ёмкости крови и сердечного выброса, необратимым метаболическим нарушениям, «шоковым» повреждения органов с развитием полиорганной недостаточности и летальному исходу.
В патогенезе гиповолемического шока необходимо учитывать и роль развивающегося дисбаланса электролитов, в частности, концентрацию ионов натрия в сосудистом русле и внеклеточном пространстве. В соответствии с их концентрацией плазме крови выделяют изотонический тип дегидратации (при нормальной концентрации), гипертонический (повышенная концентрация) и гипотонический (пониженная концентрация) тип обезвоживания. При этом, каждый их этих типов обезвоживания сопровождается специфическими сдвигами осмолярности плазмы, а также внеклеточной жидкости, что оказывает существенное влияние на характер гемоциркуляции, состояние сосудистого тонуса и функционирование клеток
И это важно учитывать при выборе схем лечения
II. Кардиогенный шок
Кардиогенный шок – является реогемодинамическим и метаболическим отражением выраженного повреждения миокарда с недостаточностью его насосной функции в результате неадекватного коронарного кровотока, заболеваний миокарда или перикарда, клапанных поражений или от сочетания этих причин.
Этиология
Выраженное снижение сердечного выброса может развиться при различных нарушениях сердечного ритма, снижения сократительной способности миокарда (ишемия и инфаркт миокарда, миокардит, миокардиопатия), при повреждении структур сердца (митральная или аортальная регургитация, разрыв межжелудочковой перегородки, повреждение искусственных клапанов), механических препятствиях венозному оттоку или наполнению желудочков (напряженный пневмоторакс, пережатие полой вены, тампонада сердца, опухоль сердца, опухоль предсердия или тромб), препятствиях изгнанию крови из желудочка (эмболия легочной артерии).
Наиболее часто к подобному состоянию приводит острая непроходимость коронарных артерий или контузия миокарда.
Кардиогенный шок развивается у 12−20% больных инфарктом миокарда приблизительно через 12−18 часов, а иногда спустя 2−4 дня после того, как возникла острая непроходимость коронарных артерий.
Патогенез
Кардиогенный шок развивается по патогенетическим механизмам классического шока, проходя через стадии периферических, реологических и гемодинамических расстройств.
Уменьшение сердечного выброса приводит к недостаточной перфузии органов и тканей с нарушением их функций. Компенсаторные реакции в виде активации симпатоадреналовой и ангиотензин-альдостероновой активности повышают потребность организма, в том числе и самого миокарда, в кислороде, что еще в большей степени отягощает гипоксию.
В результате происходит повреждение эндотелия с выделением значительного количества медиаторов и цитокинов с нарастанием апоптоза и некроза клеток в органах.
Различают две формы кардиогенного шока:
– Истинный кардиогенный шок – развивается при существенном ограничении сократительной функции миокарда, что влечет значительное ограничение микроциркуляции; подразделяется на кардиогенный шок среднетяжелой, тяжелой степени и ареактивный кардиогенный шок, при котором развивается тотальная блокада микроциркуляторного русла.
– Аритмогенный кардиогенный шок, который подразделяется на тахисистолический и брадисистолический. Нарушения сердечного ритма преимущественно возникают в результате нарушения водно-электролитного баланса.
Диагностика инфаркта миокарда:
– соответствующая клиническая симптоматика,
– электрокардиографические изменения,
– выявление нарушения проходимости коронарных сосудов при ангиографии или ангиоскопии,
– нарастание полиморфно-клеточного лейкоцитоза, который относится к неспецифическим показателям некроза тканей и реакции воспаления в ответ на повреждение миокарда,
– повышение уровня креатинфосфокиназы, лактатдегидрогеназы, аспартатаминотрансферазы и аланинаминотрансферазы сыворотки крови,
– повышение уровня миоглобина и тропонинов в крови,
– изменение коэффициента де Ритса (нарастание соотношения аспартатаминотрансферазы, аланинаминотрансферазы).
Клиническая картина
Основными клиническими проявлениями кардиогенного шока являются беспокойство больного, выраженная бледность кожных покровов с холодным липким потом, выраженным болевым синдромом, характеризующимся «тяжелыми», «сжимающими», «разрывающими» болями за грудиной, болевые ощущения могут возникать в эпигастральной области или иррадиировать в верхние конечности, нижнюю челюсть, левую половину шеи. Развиваются тошнота и рвота, различные нарушения сердечного ритма на фоне бради- или тахикардии, артериальное давление критически снижается, возникают олигоанурия, гипоксемия, метаболический ацидоз.
Общие направления лечения шока
Лечебные мероприятия в первую очередь должны быть направлены на устранение или минимализацию шокогенного фактора и коррекцию патофизиологических нарушений, которые возникают как ответная реакция на снижение циркуляции, гипоперфузию, нарушение клеточного обмена.
Очередность проводимых лечебных мероприятий зависит от основной причины, которая спровоцировала шоковое состояние:
− устранение или минимализация влияния на организм причин, вызвавших шоковое состояние (применение кровоостанавливающего жгута, иммобилизация поврежденной конечности, восстановление проходимости дыхательных путей, устранение или ограничение очага инфекции, прекращение контакта с веществом, которое спровоцировало анафилактический шок, восстановление проходимости сосуда, аорто-коронарное шунтирование);
− восполнение, поддержание соответствующих реологических характеристик и должного объема циркулирующей крови, возобновление микроциркуляции, кровоснабжения органов и тканей;
− устранение ацидоза (потому, что фармакотерапия наиболее эффективна только при физиологических значениях pH), восстановление водно-солевого и белкового баланса;
− поддержание нормального функционирования органов и систем, при необходимости проводить их временное замещение (искусственная вентиляция легких и кровообращение, детоксикация);
− поддержание нормальной температуры тела, адекватное обезболивание на фоне восстановления жидкостных разделов организма и устранения гиповолемии;
− обеспечение метаболических потребностей организма (парентеральное питание);
− специфическая медикаментозная интенсивная терапия (применение антибиотиков, гормонов, вазопрессорных фармпрепаратов, препаратов крови и кровезамещающих растворов).
При беременности
Геморрагический шок в акушерстве, возникающей при вынашивании беременности, в родовом акте, а также в раннем/позднем последовом периоде являются одной из значимых причин в структуре материнской смертности на долю которого приходится около 20–25%. Показатель акушерских кровотечений относительно общего числа родов варьирует в пределах 5-8%.
Спецификой кровотечений в акушерстве являются:
- Внезапность их появления и массивность.
- Высокий риск гибели плода, что обуславливает необходимость срочного родоразрешения до момента стойкой стабилизации показателей гемодинамики и завершения инфузионно-трансфузионной терапии в полном объеме.
- Сочетанность с резко выраженным болевым синдромом.
- Быстрое истощение компенсаторно-защитных механизмов. При этом, особенно высокий риск у беременных поздним гестозом и у женщин с осложненным течением родов.
Допустимая кровопотеря в родах при их нормальном течении не должна превышать 250-300 мл (ориентировочно 0,5% массы тела женщины). Такой объем кровопотери относится к «физиологической норме» и не отражается негативно на состоянии роженицы. Основными причинами острой патологической кровопотери при беременности с развитием геморрагического шока являются: внематочная беременность, отслойка/предлежение плаценты, многоплодная беременность, осложнения в течении родов, кесарево сечение, разрыв матки.
К особенностям геморрагического шока при акушерской патологии относятся: частое его развитие на фоне тяжелой формы гестоза беременных, быстрое развивитие гиповолемии, синдрома ДВС, артериальной гипотензии, гипохромной анемии.
При ГШ, развившемуся в раннем послеродовом периоде на фоне гипотонического кровотечения, характерен краткий период неустойчивой компенсации, после чего быстро развиваются необратимые изменения (стойкие нарушения гемодинамики, синдром ДВС с профузным кровотечением, дыхательная недостаточность и нарушением факторов свертывания крови с активацией фибринолиза).